[拼音]:biding
[外文]:pyridine
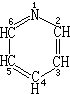 含有一个氮杂原子的六元杂环化合物,即苯分子中的一个-CH=被氮取代而生成的化合物,故又称氮苯,分子式H5H5N。 吡啶最初由骨焦油内分离出来,随后发现煤焦油、煤气、页岩油、石油内也含有吡啶及其同系物,如2-甲基吡啶和2,6-二甲基吡啶。
含有一个氮杂原子的六元杂环化合物,即苯分子中的一个-CH=被氮取代而生成的化合物,故又称氮苯,分子式H5H5N。 吡啶最初由骨焦油内分离出来,随后发现煤焦油、煤气、页岩油、石油内也含有吡啶及其同系物,如2-甲基吡啶和2,6-二甲基吡啶。
性质
吡啶为无色的可燃液体;具有特殊臭味;熔点-42℃,沸点115.5℃,密度0.9819克/厘米3(20℃);与水形成共沸混合物,其沸点为92~93℃。工业上利用这个性质来纯化吡啶。吡啶具有接近正六角形的结构,与苯类似,具有相同的电子结构。按照共振论,吡啶至少是下列几种不同的极限式的杂化体:

c和d两个极限式代表两个极性的结构,这与吡啶具有很大的偶极矩是符合的。
吡啶及其衍生物比苯稳定,其反应性与硝基苯类似。由于环中氮原子的吸电子作用,使2,4,6位上的电子密度低于3,5两位,典型的芳香族亲电取代反应发生在3,5位上,但反应性比苯低,一般不易发生硝化、卤化、磺化等反应。此外,这些取代反应都是在酸性介质内进行的,吡啶形成带正电荷的离子, 使亲电试剂不易接近。2-或4-卤代吡啶的卤素都具有活性。由于2和6位上的电子密度较低,在此位上可发生亲核取代反应,如与氨基钠或氢氧化钾反应,得到相应的2-氨基吡啶或2-羟基吡啶。
吡啶是一个弱的三级胺,在乙醇溶液内能与多种酸(如苦味酸或高氯酸等)形成不溶于水的盐。工业上使用的吡啶中约含1%的2-甲基吡啶,因此可以利用成盐性质上的差别,使它和它的同系物分离。吡啶还能与多种金属离子形成结晶形的络合物。
吡啶比苯容易还原,如在金属钠和乙醇的作用下,还原成六氢吡啶(或称哌啶)。吡啶与过氧化氢反应,容易被氧化成N-氧化吡啶:

N-氧化吡啶是一个重要的吡啶衍生物,由于氮原子被氧化后,不能再形成带正电荷的吡啶离子,因此有利于发生芳香族亲电取代反应,取代完毕后,再将氮上氧除去,就可以得到由吡啶直接取代所不能得到的衍生物。
制法
吡啶可以从炼焦气和焦油内提炼。将炼焦气通过硫酸,吸收其中的氨和吡啶等含氮的碱性物质,用氨气处理所产生的硫酸铵盐类的溶液,分出游离的含氮有机碱类,然后蒸馏,即得到吡啶及其烷基取代物的混合液。吡啶及其衍生物可以通过多种方法合成。其中应用最广的是汉奇吡啶合成法,这是用两分子的β-羰基化合物,如乙酰乙酸乙酯与一分子乙醛缩合,产物再与一分子的乙酰乙酸乙酯和氨缩合形成二氢吡啶化合物,然后用氧化剂(如亚硝酸)脱氢,再水解失羧,即得吡啶衍生物:

应用
吡啶的许多衍生物中,有些是重要的药物,有些是维生素或酶的重要组成部分。例如吡啶-3-羧酸的酰胺(即烟酰胺),在辅酶I中与腺嘌呤(见嘌呤)、核糖及磷酸形成一个重要的二核苷酸。吡啶的衍生物异烟肼是一种口服的抗结核病药。2-甲基-5-乙烯基吡啶是合成橡胶的重要原料。
