[ƴ��]��eryanghuatan
[����]��carbon dioxide
��ѧʽCO2����ɫ��������ζ�������壻�۵�-56.6�棨5.2����ѹ�����ܶ� 1.977 �ˣ������ٽ��¶�31.04�棬�ٽ�ѹ�� 72.85����ѹ�� ��ˮ�е��ܽ��Ϊ0.1449��/100��ˮ(25��)����20��ʱ����������̼��ѹ��59����ѹ����Һ����Һ̬������̼Ѹ���������������Ȼ�ʹ��һ�����������䣬�γ�ѩ��״���壬���ֹ�������ʱ������Һ�壬�׳ơ��ɱ�����

������̼��ֱ���ͷ��ӣ��ṹʽ��������C��O����Ϊ1.16��������Ϊ531.4ǧ��/Ħ�������ӵ�ż����Ϊ0���ǷǼ��Է��ӡ�������̼�кܸߵ����ȶ�����ֻ�ڸ����²ŷֽ��һ����̼������
��ѧ����������̼Ϊ�������������ˮ����̼��������������ʽ̼������̼���Σ�
CO2+H2O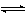 H2CO3
H2CO3
CO2+OH-����HCO�A
CO2+2OH-����CO��+H2O
������̼�ڳ���̿�������»�ԭ��һ����̼��
CO2+C����2CO
�ڼ����£�������̼������ý�������̼��̼���λ����������磺
4K+3CO2����2K2CO3+C
2Mg+CO2����2MgO+C
������̼����ˮ����ˮ��������Ѹ������װ����ã��ֱ�����������������̼������

������̼�����백���ã����ɰ���̼���������190����ѹ�¼��ȵ�180��ʱת������أ�

����ˮ�����£�������̼�백����̼����泥�
NH3+CO2+H2O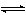 NH4HCO3
NH4HCO3
����̼��̼�Ŀ�ȼ���ڳ����������ȼ�տɲ���������̼���л���ĸ��ú��ˡ���ĺ���Ҳ�ɲ������ų�������̼���ڹ�ҵ�ϣ�������̼������ʯ��ʯ��ȡʯ�һ��������ĸ���Ʒ��Ҳ�������������ͺ�����������Ʒ�����࣭����ת��¯�ĸ��������Ȼ������ú������¯��Ҳ�ɵõ������Ķ�����̼��
��ʵ��������������ʯ��ʯ��������ʯ����Ӧ����ȡ������̼��
CaCO3+2HCl����CaCl2+H2O+CO2
��ʱ�̵�����Ҳ����������̼����Դ����ȥ�����̡�̿���ķ�����ȴ��ͨ��Ũ��̼�����Һ�������ն�����̼������ʱֻҪ����Һ���ȼ��ų�������̼��
Ӧ��������̼���������������С�մ���������Ǧ�ס����غ�̼����淋ȣ���������������Һ����Ե��Լ����������ϵijɷ֡����������ʼ���������ȡ�������̼���������˹�ģ������������о���ũҵ�����С�
������̼���ԣ��ڴ����к���Ϊ0.03������������ң�ijЩ�ֲ�������ӵ������������ߴ�1�����ڿ����еĺ����ﵽ3��ʱ�������е��������٣���Ũ�ȴﵽ10��ʱ���ͻ�ɥʧ֪��������ֹͣ��������
�����
- ����Ⱦ����в���ڶ�����̼��̬��ȫ
- ���������̼�ж�������Щ֢״�����Ԥ����ʳ�þ�
- ������̼�����㹽����ʳ�þ�
- ���ֶ�����̼ʩ��װ�������ڡ��زˡ��������߲���
- �ճ������ж�����̼���ŷ���̬��ȫ
- ��ʯ�Ͷ�����̼����˹��ͻ������Щ�����������ɿ�ұ��
- ���Թ����������������̼������
- ���������̼�ж�������Щ֢״���߲���
- ʲô�Ƕ�����̼��̬��ȫ
- �����������к����弰������-������̼��CO2����