[拼音]:shengwu yanghua
[外文]:biological oxidation
代谢物脱下的氢及电子,通过一系列酶促反应与氧化合成水,并释放能量的过程。生物氧化过程出现障碍,或其产生的能量不能保留为ATP,均将严重危害机体的健康,这也是许多抗菌药物的机理所在。生物在生活过程中不停地消耗能量,当然必须有能量的供给,能量的基本来源是食物。经过消化吸收的食物和一小部分体内原有的组成成分,在细胞内进行降解,释出所蕴藏的能量以供生命活动的需要。最基本的释放能量的反应是氧化作用。生物体内的氧化作用与能量的生成有其特点,这就称为生物氧化。
若使体内的各种代谢物质在体外进行氧化,一般都需高温或酸硷等强烈条件方能进行;由分子氧直接氧化代谢物上的氢及碳,分别生成最终氧化产物H2O及CO2,同时骤然放出大量热能,其能量通常难于被有效利用。如:

而生物氧化则是在一系列酶的催化下完成的,反应条件温和,温度近于体温, 酸碱度近于中性。 生物氧化并非代谢物与氧直接结合,而以脱氢为主。首先是在酶的作用下,氢原子失去电子变成H+,再脱下来,逐步脱氢(氧化的一种方式),脱羧(脱CO2的一种方式),脱下的氢在线粒体中,经一连串的递氢体和递电子体组成的呼吸链的传递,最后同氧结合成水。在此氢和电子传递过程中,逐步释出能量,不会产生高热。根据可逆过程可做最大功的原则,部分释出的能量可以转化成三磷酸腺苷 (ATP)中的高能磷酸键的化学能形式,供体内各种生理、生物化学活动的需要。如

可见,体内吸入氧气是为了接受经呼吸链传递而来的氢或电子,而非直接用于氧化代谢物上的氢。脱羧作用所生成的CO2则是呼气中CO2的主要来源。值得注意的是,葡萄糖在体内氧化所释出的总能量与体外氧化者完全等同,均为686千卡。但体外氧化所释出的能量全部以热能的形式散失;而体内氧化所释出的能量中,则有一部分(约262千卡)可转化为ATP的形式,供做有用功之用,其余散发为热。
糖、脂肪、蛋白质在体内氧化降解的过程
在体内,糖、脂肪和氨基酸(蛋白质的组成成分)经过各种脱氢酶催化的脱氢反应,脱羧酶催化的脱羧反应,以及为脱氢、脱羧作准备的一系列酶促转变,不同长度的碳链断裂降解成二碳单位(乙酰辅酶 A)。然后此二碳单位再经三羧酸循环的一系列酶促化学转变,加水脱氢、脱羧而被完全降解成CO2及氢(图1)。

经各种脱氢酶催化脱下的氢被脱氢酶的辅酶所接受,然后经呼吸链的传递,最后统统交给氧生成水。一个在安静状态下体重为70kg的成人,每分钟耗氧264ml,每分子氧接受2原子氢或2个电子;则经脱氢酶和呼吸链传递的电子数多达每分钟2.86×1022,据推算,以此电流所做的功相当于100W的电机所做的功。
生物氧化的酶类及氢和电子传递体
生物氧化过程包括脱氢酶激活氢,氧化酶激活氧,以及一连串递氢体和递电子体组成的呼吸链中介。
氧化酶这类酶的辅基多含金属离子,能利用代谢物上的电子激活分子氧并使之与氢结合成水。如广泛分布于各种哺乳动物细胞中的细胞色素氧化酶,它的辅基是铁卟啉,并含铜离子。它对氰化物有极大的亲和力,少量氰化物即可抑制该酶的活性,导致细胞内呼吸抑制而使机体死亡。
脱氢酶可分为两类:
(1)需氧脱氢酶。是以黄素核苷酸(FMN或FAD)为辅基的一类黄素蛋白。它催化代谢物脱氢,脱下的氢转交给氧原子,生成过氧化氢。它不产生可做有用功的能。例如催化神经递质儿茶酚胺、5-羟色胺等单胺类化合物氧化脱氨基的单胺氧化酶即属于需氧脱氢酶。抑郁症患者神经突触中的儿茶酚胺类含量减少,临床上可应用单胺氧化酶抑制药,以阻断单胺氧化酶对这类神经递质的氧化降解,使症状得以改善。
(2)不需氧脱氢酶类。能使作用物的氢活化,又不以氧为受氢体,而由辅酶或辅基作为受氢体。这些辅酶或辅基包括有辅酶Ⅰ(烟酰胺腺嘌呤二核苷酸,NAD+),辅酶Ⅱ(磷酸烟酰胺腺嘌呤二核苷酸,NADP+)、 FMN或FAD等。这些辅酶接受氢后,将氢或电子通过呼吸链传递,经氧化酶的催化,交给氧生成水。例如,葡萄糖代谢的重要中间步骤,催化三磷酸甘油醛脱氢的脱氢酶系以辅酶Ⅰ为受氢体。此酶可被重金属离子、烷化剂及砷酸根所抑制,这也是这些毒物中毒的机理之一。
递氢体和递电子体组成呼吸链的成分包括各种递氢体和递电子体。
(1)辅酶Ⅰ(NAD+)和辅酶Ⅱ(NADP+)。它们为烟酰胺核苷酸,其分子中烟酰胺上的吡啶氮为五价,能够可逆地接受电子而变为3价,失去电子而回复为5价。其对位的碳原子也比较活泼,能可逆地加氢和脱氢。
(2)黄酶。以FMA或FAD为辅基,系黄素核苷酸,其分子中的异咯嗪上的两个氮原子部位可以可逆地加氢和脱氢。
(3)铁硫蛋白(Fe2S2)。含有非血红素铁与硫。铁硫蛋白中铁原子为3价,两个铁原子中只有一个铁原子可以接受电子成2价铁。
(4)辅酶Q。系生物界广泛分布的一类醌类,其分子中的醌部分能可逆地接受氢而成氢醌。
(5)细胞色素。一类以铁卟啉为辅基的结合蛋白质,可根据吸收光谱的不同,分为三组细胞色素,即细胞色素a、b和c,其中a又可区分为a和a3等,a3能直接激活氧接受电子,故又称为细胞色素氧化酶。c又可区分为 c1、c 等。细胞色素分子中铁卟啉上的铁能可逆地氧化还原,接受电子而被还原成Fe2+,或放出电子而被氧化为Fe3+。
呼吸链的组成
参与生物氧化的递氢体和递电子体高度有序地组装在线粒体内膜上,主要按它们的氧化还原电极电位递增的顺序排列。因为电子由低电位流向高电位,所以电位低的物质容易失去电子而被氧化,电位高的物质容易获得电子而被还原。现已基本研究确定的呼吸链中的电子传递顺序(图2)。
 NADH氧化呼吸链
NADH氧化呼吸链
生物氧化过程中绝大多数脱氢酶以 NAD+ 为辅酶, NAD+ 接受代谢物上脱下的两个氢原子成 (NADH+H+), 以后又依次将氢或电子传递给 在传递过程中细胞色素只接受电子,而将质子(H+)游离于介质中,最后经过aa3将电子传给氧原子,生成O2-,然后O2-即与介质中的 2H+化合成水。各递电子(氢)体在线粒体内膜上的排列见图3。
在传递过程中细胞色素只接受电子,而将质子(H+)游离于介质中,最后经过aa3将电子传给氧原子,生成O2-,然后O2-即与介质中的 2H+化合成水。各递电子(氢)体在线粒体内膜上的排列见图3。
 琥珀酸氧化呼吸链
琥珀酸氧化呼吸链
琥珀酸是三羧酸循环中的一个重要环节,在琥珀酸脱氢酶的催化下,以 FAD为受氢体,形成FADH2,然后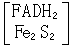 再依次把氢或电子传递给辅酶
再依次把氢或电子传递给辅酶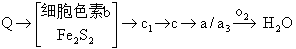 。用于杀死鱼类和日本血吸虫的鱼藤酮,以及巴比妥类催眠药可抑制
。用于杀死鱼类和日本血吸虫的鱼藤酮,以及巴比妥类催眠药可抑制 见环节,所以鱼藤酮中毒时NADH氧化呼吸链受抑制;但琥珀酸氧化呼吸链仍通畅。抗霉素抑制细胞色素b→c1的电子传递;氰化物抑制细胞色素a3,所以它们能同时阻断两条氧化呼吸链,而致哺乳动物于死地。
见环节,所以鱼藤酮中毒时NADH氧化呼吸链受抑制;但琥珀酸氧化呼吸链仍通畅。抗霉素抑制细胞色素b→c1的电子传递;氰化物抑制细胞色素a3,所以它们能同时阻断两条氧化呼吸链,而致哺乳动物于死地。
氧化磷酸化
在氢或电子沿呼吸链传递至氧生成水的过程中,能量逐步释出,部分能量促使 ADP+Pi→ATP(二磷酸腺苷 +无机磷酸→三磷酸腺苷),以高能磷酸键的形式将能量保存在 ATP中。这两个过程是紧密偶联的,若无电子沿呼吸链的下传,则无ADP磷酸化成ATP;但若组织中有限的ADP均被磷酸化成ATP,而ATP又不能被耗用时,则电子沿呼吸链的下传也将不能进行,以节制能量。2,4-二硝基酚(DNP)则能拆离它们的偶联,使营养物大量被氧化脱氢,经呼吸链与氧化合成水,其释放出的能量不能保留为ATP,而被散失为热能,因此曾作为减肥药物。
现已研究确定在呼吸链上与氧化磷酸化偶联的部位有三处:
(1)自NADH→辅酶Q;
(2)自细胞色素b→细胞色素c1;
(3)自细胞色素a/a3→O2。当一对氢(或电子)沿呼吸链下传时,在此三处释放的能量较多,可分别与ADP+Pi→ATP的过程相偶联,分别生成一分子ATP。所以当一对氢(或电子)沿NADH氧化呼吸链传递时,可生成三分子ATP;而若系沿琥珀酸氧化呼吸链传递,则只生成二分子ATP。呼吸链传递电子时释出的能量何以能驱动 ADP+Pi→ATP,迄今尚未完全阐明,比较满意的解释是米切尔氏(1961)的化学渗透学说。这一学说认为,呼吸链存在于线粒体内膜上,当氢或电子沿呼吸链传下去时,同时驱动氢离子由线粒体基质穿过线粒体内膜进入内外膜间的膜间腔。因为氢离子不能自由通透线粒体脂质内膜,从而建立了跨膜的电化学质子梯度。这个质子梯度包含氢离子浓度差 (△pH)和电位差(△E),这个梯度就蕴藏着电子传递过程中所释出的能量。然后,当氢离子经位于线粒体内膜上的F1-F0-ATP 酶复合物构成的特殊通道(图3),渗透进入膜内时,驱动ADP+Pi→ATP。
偶联拆离剂2,4-二硝基酚(DNP)可与线粒体膜外的质子结合,并直接通过脂质内膜进入基质,从而破坏了内膜两侧的质子梯度,使氧化磷酸化不能进行。寡霉素则可与内膜上F1-F0-ATP酶的F0部分结合,抑制了ATP酶的活性,使ADP+Pi→ATP的过程不能进行。甲状腺功能亢进者的基础代谢率增高,产热增多,这是因为甲状腺素能促进细胞膜上Na+、K+-ATP酶的合成,此酶是促使ATP分解的酶,从而促使ATP加速分解为ADP和磷酸,并将其化学能散失为热能。ADP的生成增多又反过来促进ATP的合成和分解增强,以及呼吸链的加速进行,于是出现耗氧量和产热量的增加。
ATP的来源、储存和利用
体内各种生理活动的能量来源,直接或间接的由ATP提供,如肌肉收缩需要ATP的水解供能,阳离子(如Na+、Ca2+、H+)在细胞膜内外的主动转移,蛋白质及核酸等生物大分子的生物合成及代谢物的磷酸化等等都无不有赖于ATP提供能量。ATP主要由氧化磷酸化生成;也可直接由代谢物分子中的高能磷酸键转移至ADP,以合成ATP,但后者只占ATP生成总量的一小部分。如在葡萄糖无氧分解时的重要中间产物 1,3-二磷酸甘油酸上的1位高能磷酸键,可转移给ADP以生成ATP。
当ATP水解成ADP及磷酸时,约可释出7.5千卡可供利用的能量。既然体内各种生命活动都离不开 ATP提供能量,但体内ATP的实际含量又极少(不足1g),据估计只够维持2秒钟的活动;而一个安静状态的成人一天约需消耗40公斤的ATP,若剧烈运动则每分钟所消耗的ATP量多达0.5公斤。因此,一方面需要不断的通过ADP匑ATP源源不断地再生ATP。ADP的积累可刺激氧化磷酸化过程,生成更多的ATP。另一方面肌肉及脑组织中富含磷酸,磷酸肌酸是体内高能磷酸的储存形式,其高能磷酸键系由ATP转移给肌酸所合成,它不能直接利用以支持生理生化作用,只是当机体消耗大量ATP而导致ADP增多时,磷酸肌酸分子中的高其高能磷酸键方能转移给ADP而合成ATP,以供生理活动的需要。
生物氧化的其他类型
生物氧化的主要方式是脱氢,并将氢经呼吸链的传递与氧化合成水,这是体内产生能量的主要途径。有些物质也可经其他类型的生物氧化以氧化之,这并不产生可供做功的能,但有一定的生理意义。例如:
加氧酶类反应体系这类酶催化氧原子加入代谢物中,形成加氧化合物。如肝细胞微粒体中存在有加单氧酶体系,可使许多代谢物、药物及毒物通过羟化(即加氧)而进行生物转化,使其转变成生物学活性或非活性物质,或增加其极性和水溶性,易于排出体外。如解热镇痛药非那西汀是一种中性脂溶性化合物,水中溶解度低。经肝中微粒体加氧转变后,增加了亲水性,才易于被清除。又如血红素也须先经微粒体加氧酶的作用以破坏而生成胆绿素,再代谢转变成胆红素。其他如胆固醇的转变成肾上腺皮质激素或性激素,维生素D的活化等无不有加氧酶的参与。
过氧化物酶和过氧化氢酶反应体系这些酶能使过氧化氢分解,生成水,从而消除体内生成的过多过氧化氢的有害作用。在某些组织中,氧化过程中产生的过氧化氢有其他积极的生理意义。例如嗜中性粒细胞产生的过氧化氢可用于杀死吞噬进来的细菌。甲状腺中产生的过氧化氢可用于酪氨酸的碘化以合成甲状腺素。有的组织在氧化过程中可生成超氧化基团(O娛),超氧离子对细菌等具杀伤作用,但同时也能危及细胞的生命活动。通过超氧化物歧化酶可将O娛转变成过氧化氢,然后经过氧化物酶以清除之。老年时超氧化物歧化酶的活力降低,这可能是促进衰老的因素之一。