[拼音]:yangshi tu
[外文]:oxygen-potential diagram
又称氧位图。稳定单质(M)与1摩尔氧结合成氧化物(MxOy)的反应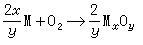 的标准自由焓变量ΔG°(即氧势) 与温度T的关系图。1944年,埃林汉(H.J.T.Ellingham)首先将许多氧化物的ΔG°对T 作图,得到一系列直线,所以称为埃林汉图。1948年里恰桑(F.D.Richardson)等人在此图上增加了氧分压及p啹 /p喅,pCO/p哘标尺,扩大了此图的应用范围,故又称为埃林汉-里恰桑图。以后,虽然有许多学者根据更可靠的热力学数据对该图作了修订补充,但图的形式并没有原则性的变化,图是奥利特(M.Olette)等人绘制的ΔG°-T图。
的标准自由焓变量ΔG°(即氧势) 与温度T的关系图。1944年,埃林汉(H.J.T.Ellingham)首先将许多氧化物的ΔG°对T 作图,得到一系列直线,所以称为埃林汉图。1948年里恰桑(F.D.Richardson)等人在此图上增加了氧分压及p啹 /p喅,pCO/p哘标尺,扩大了此图的应用范围,故又称为埃林汉-里恰桑图。以后,虽然有许多学者根据更可靠的热力学数据对该图作了修订补充,但图的形式并没有原则性的变化,图是奥利特(M.Olette)等人绘制的ΔG°-T图。
 氧势
氧势
金属氧化反应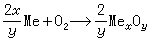 达到平衡时的氧分压pO2 称为化合物MexOy的分解压,此值越低,表示金属氧化物MexOy越稳定,它与氧化反应的ΔG°的关系是:ΔG°=R T ln pO2
达到平衡时的氧分压pO2 称为化合物MexOy的分解压,此值越低,表示金属氧化物MexOy越稳定,它与氧化反应的ΔG°的关系是:ΔG°=R T ln pO2
式中R为气体常数,T为绝对温度。当气相中氧的分压为pO2时,其化学势是:μO2 =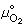 +R T ln pO2
+R T ln pO2
式中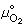 是氧分压为1大气压时的标准化学势。μO2与
是氧分压为1大气压时的标准化学势。μO2与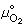 之差:μO2-
之差:μO2-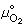 =R TlnpO2=ΔG°代表此平衡体系中氧的相对化学势,常简称为氧势(oxygen potential)。
=R TlnpO2=ΔG°代表此平衡体系中氧的相对化学势,常简称为氧势(oxygen potential)。
图中的纵坐标ΔG°也就是氧势坐标,故此图称为氧势图。ΔG°-T直线的斜率取决于反应的熵变ΔS°的符号及数值:

在相变温度,ΔG°-T直线发生转折。由于气体的摩尔熵比凝聚相的摩尔熵大得多,金属单质与1摩尔氧气反应生成凝聚相氧化物的熵变总是负值,所以它们的 ΔG°-T直线斜率为正。碳与 1摩尔氧气反应生成CO2(1大气压)气体时,由于消耗1摩尔气体(O2)生成1摩尔气体(CO2)反应的熵变极小,其ΔG°-T直线的斜率几乎为零。碳与1摩尔氧气反应生成2摩尔CO气体的ΔG°-T直线的斜率为负,表明温度越高,碳能创造更低的氧势。此线可以和其他斜率为正的直线相交。此交点温度称为氧化-还原的转化温度,在此交点温度以上,碳可以将该氧化物还原,表明碳在高温下有很强的还原能力,这就是碳成为火法冶金中最重要的还原剂的理论根据。当CO分压低于 1气压时,其ΔG-T直线(图中未给出)的斜率更负,它与其他斜率为正的直线的交点温度更低,在低压下碳更易于将各种金属氧化物还原,这是真空碳热还原的热力学依据。
 氧势图的应用
氧势图的应用
氧势图对火法冶金过程氧化物还原反应的热力学判断很有用。它能直观地表明各种氧化物稳定性的次序。图中直线位置越低,它所代表的氧化物越稳定。如含有FeO、MnO、Cr2O3、V2O3的一组冶金原料,欲在1300℃用碳处理,则可由氧势图一目了然地看出,在pCO为1大气压条件下,FeO、Cr2O3会被碳还原,而MnO及V2O3不会被还原。
利用氧势图右边所附的氧压标尺,p啹 /p喅及pCO/p哘标尺可以直接读出在一定温度下氧化物和金属平衡时的氧分压以及平衡时的p啹 /p喅及pCO/p哘值。例如,欲求NiO在1200℃的分解压,可在NiO的ΔG°-T 直线上找到1200℃的位置点,将此点与左上角的Ω点连成直线并外延到与右边pO2标尺相交,则交点处给出的氧分压7.5×10大气压,即为NiO的分解压。类似地,可将上述位置点与图左边的H点连成直线并外延到与右边的p啹 /p喅标尺相交,则交点处给出的p啹 /p喅值为1/102,这就是1200℃下与NiO、 Ni平衡的气相中氢和水蒸气分压的比值。仿此,欲求平衡的pCO/p哘值,则应与左边的C点相连接。这些标尺的利用,给控制氧化还原气氛带来很多方便。
对其他类型化合物,诸如硫化物、氯化物、碳化物、氮化物等,相应地也有硫势、氯势、碳势、氮势等概念,可绘出类似的硫势图、氯势图、碳势图、氮势图等。这些图在冶金中均已得到广泛应用,不过只适用于标准态下的反应。