[中图分类号]X5[文献标识码]A[文章编号]1007-1865(2011)12-0077-03
磷在自然界的循环是人们极为关注的问题,因为磷一方面是生态系统中必不可少的营养元素,另一方面大量的磷会导致水体的富营养化,使生态平衡遭到破坏。沉积物对上覆水中磷的含量起缓冲作用,随着环境条件的改变,沉积物中的磷可以进入间隙水中,进而通过扩散作用,在上覆水中重新参与磷循环。同时水体中的磷可与水中共存的离子,如铁、铝和钙等离子相结合以不同的结合态共存于沉积物中。当水体中氮和磷的浓度比在10∶1~25∶1的范围时,藻类生长与氮磷浓度存在直线相关关系。水体富营养化已成为当今世界水污染治理难题。当水体中磷元素供应充足时,有利于藻类生长,促使水体迅速向富营养化方向发展。因此,磷元素是水体富营养化的限制因子,故研究水体除磷技术与方法对控制和治理水体富营养化是十分重要的。除磷的方法主要分为物理法、化学法及生物法三大类。物理法因成本过高、技术复杂而很少使用。生物法除磷是新工艺,近20年来得到了广泛的重视和研究。但这种工艺一般用于污水处理厂,对于自然水体,生物法存在一定的局限性。化学法是最早采用的一种除磷方法,它是以磷酸盐能和某些化学物质如铁盐、铝盐、石灰等反应生成不溶的沉淀物为基础进行的,其产物常有絮凝的作用,有助于磷酸盐的分离。这种方法也大都用在污水处理厂的工艺上。文章用化学方法处理富营养化自然水体,旨在控制水花的发生,避免因水花的大量爆发而发生大的生态危害。
1.材料与方法
实验水样采自荆州东门护城河,采集时现场测定水样的温度与pH,拿回实验室后直接处理,或在冰箱内暂时保存。水样的pH均在7~8,水体呈墨绿色,水中丝状植物较多,有肉眼可见的细小动物游动。实验前先让其稳定沉淀后再进行处理。磷的测定按中华人民共和国国家标准GB11893-89钼酸铵分光光度法。
2.结果
2.1不同化学试剂的除磷效果
2.1.1氢氧化钙的不同投加量对除磷效率的影响
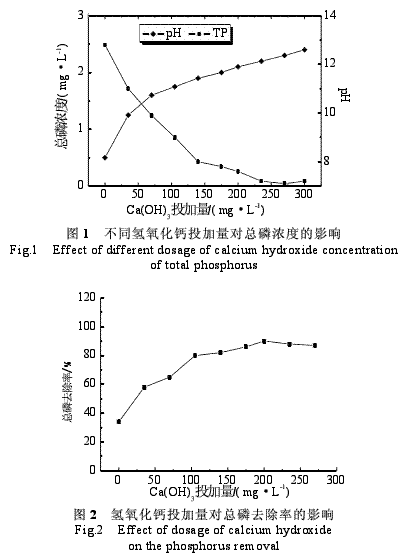
由图1可以看出,随着氢氧化钙投加量的增加,水样的pH逐渐升高,总磷含量也逐渐降低,当氢氧化钙的投加量增加到205.9mg/L后,pH和总磷浓度的变化就不再明显。由图2可知当氢氧化钙的投加量为205.9mg/L时,总磷(TP)的去除率最高(96.4%),此时的pH是11.3。当氢氧化钙的投加量超过205.9mg/L后,总磷去除率变化不明显。
2.1.2三氯化铝的不同投加量对除磷效率的影响
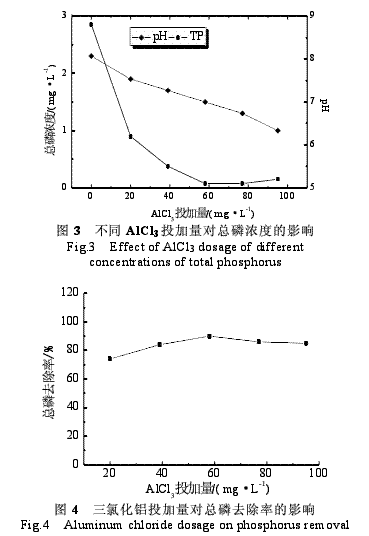
由图3可知,当三氯化铝的投加量为76.9mg/L时,TP含量最低,即总磷的去除率最高(97.7%),此时pH为6.6。但当三氯化铝的投加量为58.3mg/L时,总磷的去除率便达到了97.2%,此时pH为6.9。故最佳投加量可以确定为58.3mg/L。随着投加量的增加,处理后水样的pH逐渐降低,总磷的浓度也逐渐降低。当投加量超过58.3mg/L后,总磷的浓度变化不明显,但pH继续下降;由图4可以看出,随着三氯化铝投加量的增加,水样中磷的去除率逐渐升高,当投加量达到58.3mg/L后,总磷去除率达到最高,随后总磷去除率变化不明显。
2.1.3三氯化铁的不同投加量对除磷效率的影响
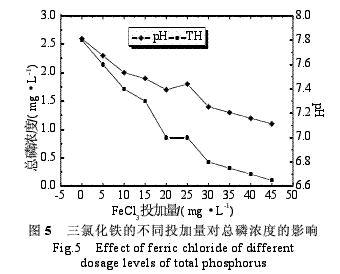
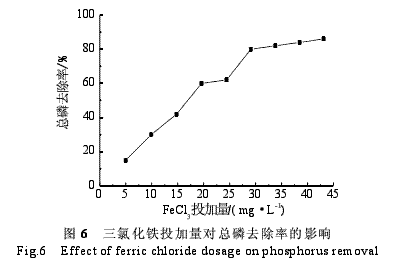
由图5和图6可知,当三氯化铁投加量为43.1mg/L时总磷浓度最低,总磷的去除率达到最高(92.1%),此时pH为7.1。而且随着三氯化铁投加量的增加,pH和总磷的浓度逐渐降低,水中总磷的去除率逐渐增加。
2.2温度对各种化学试剂除磷效率的影响
2.2.1温度对氢氧化钙除磷效率的影响
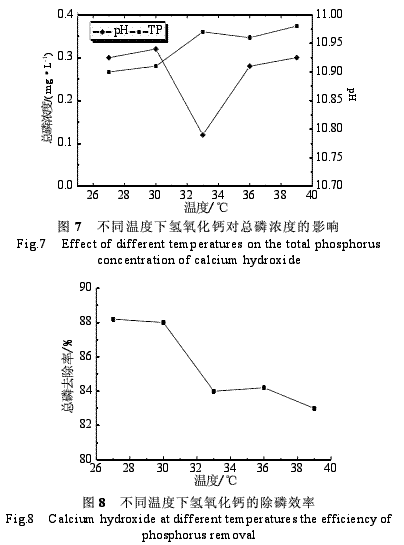
由图7可以看出,随着温度的升高,水样中总磷的浓度逐渐升高,到33℃后开始稍有降低,但36℃后又开始升高;水温在27~30℃时pH逐渐升高,30~33℃降低,但33~36℃又逐渐升高,36~39℃之间pH变化不明显。由图8可见,随着温度的升高,氢氧化钙对磷的去除率逐渐降低,超过33℃后温度对其去除率影响不明显。
2.2.2温度对三氯化铝的除磷效率的影响
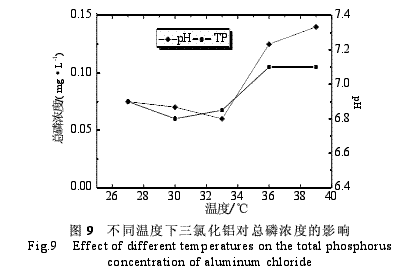
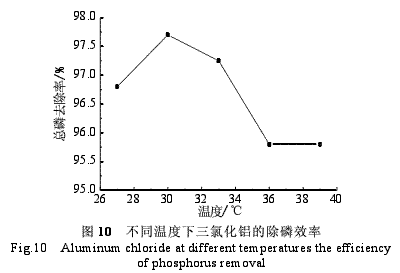
由图9和10可知,随着温度的升高,水样的pH先降低,在33℃时达到最低,然后开始升高。水中总磷的浓度也是先降低后升高,在30℃时总磷的浓度达到最低。相应的三氯化铝去磷的效率也是先升高然后降低,在30℃时总磷处理率达最高。
2.2.3不同温度对三氯化铁的除磷效率的影响
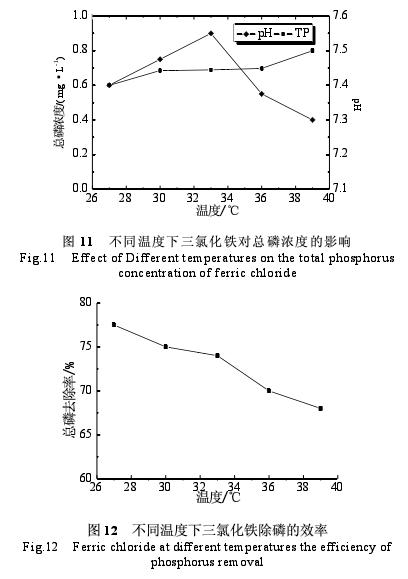
由图11和12可知,随着温度的升高,水样的pH先是升高,在33℃时升至最高,然后开始降低。而水样中总磷的浓度则随水温的升高而升高。三氯化铁除磷的效率随温度的升高而逐渐降低。
3.讨论与结论
化学除磷是通过向污水中投加无机金属盐药剂,与污水中溶解性的盐类,如磷酸盐混合后,形成颗粒状、非溶解性的物质发生化学沉析过程完成的。其中Ca(OH)2除磷的原理为:水中的磷酸根离子在有OH-存在的条件下,与Ca2+反应生成碱式磷酸钙沉淀,3HPO42-+5Ca2++4OH-→Ca5(OH)(PO4)3↓+3H2O。投加Ca(OH)2可以提高pH和Ca2+浓度,使反应向有利于生成碱式磷酸钙沉淀方向进行,使磷的去除率得到了提高。本实验结果证明了这一规律。该方法的弊端是加Ca(OH)2会导致水体pH升高。但自然水体具有一定的缓冲能力,CO2+H2O→HCO3-+H+,HCO3-+Ca2+→CaCO3↓+H+,其中H+会不断与Ca(OH)2产生的OH-结合生成H2O,从而降低水体pH。
铝盐除磷的原理一般认为是铝盐分散于水体时,一方面Al3+与PO43-反应,Al3++HnPO4(3-n)=AlPO4↓+nH+,另一方面,Al3+首先水解生成单核络合物Al(OH)2+及AlO2-等,单核络合物通过碰撞进一步缩合,进而形成一系列多核络合物Aln(OH)m(3n-m)+(n>1,m≤3n),这些铝的多核络合物促进了胶体和悬浮物等沉淀,达到较好的除磷效果。铝盐除磷可降低水体的pH,但Al对人体有毒,使用时要注意到这一点。
铁盐除磷的过程比较复杂:一方面Fe3+既可与磷酸根生成难溶盐,Fe3++PO43-=FePO4↓,又可与HCO3-结合生成Fe(OH)3沉淀,Fe3++3HCO3-=Fe(OH)3↓+3CO2;另一方面Fe3+可发生强烈水解,并发生各种聚合反应,生成具有较长线性结构的多核羟基络合物,如Fe2(OH)24+、Fe3(OH)45+、Fe5(OH)96+、Fe5(OH)87+、Fe5(OH)78+等。这些含铁的羟基络合物能有效促使胶体凝聚,通过沉淀分离将磷去除。由本实验结果可知铁盐的加入还能降低水样的pH,在pH为7左右时亦能达到较好的处理效果,而且对自然水体影响较小。
由以上分析,我们可以得出如下结论:
(1)氢氧化钙的最佳投加量在205.9mg/L,最佳反应pH为11.3,最佳反应温度为27℃;三氯化铝的最佳投加量在58.3mg/L,最佳反应pH为6.9,最佳反应温度在30℃;三氯化铁的最佳投加量为43.1mg/L,最佳反应pH为7,最佳反应温度在27℃;
(2)随着温度的升高(27~39℃),氢氧化钙和三氯化铁的除磷率明显下降,而三氯化铝的除磷率却随着温度的升高而升高,到30℃时除磷率达到最大,之后开始有所下降。可见三氯化铝比较适合在温度较高时进行处理,另两种比较适合在常温下进行处理;
(3)考虑到铝的毒性,在实际应用时采用氢氧化钙和三氯化铁单独或配合使用能达到较好的处理效果。














