[拼音]:gesuanyan
[外文]:chromates
化学通式M姟CrO4或MⅡCrO4(MⅠ为一价金属,MⅡ为二价金属)。
铬酸盐在酸性溶液中有以下平衡:

平衡常数 K=1014,表明在酸性溶液中Cr2O崻占优势;在碱性溶液中CrO娸占优势。两种离子之间的相互转化,取决于溶液的pH值。酸的浓度增大时,Cr2O崻还可进一步聚合成三铬酸盐Cr3O崠和四铬酸盐Cr4O崘。
在酸性溶液中,铬酸盐的氧化性比较明显,在碱性溶液中要弱得多:
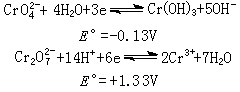
式中E°为标准电极电势(位)。实际上是重铬酸盐起氧化作用,它能氧化硫化氢、碘化氢、亚硫酸、Fe2+ 等。
重要的铬酸盐有铬酸钠 Na2CrO4和铬酸钾K2CrO4,它们都是易溶于水的黄色晶体。20℃时铬酸钠的溶解度是76.6克/100克水;铬酸钾是62.9克/100克水。钙、锶、钡、汞(Ⅰ)、银、铅的铬酸盐不溶于水,都能溶于强酸中形成重铬酸盐。利用这个特性可鉴定铬酸根离子。铬酸盐可用作氧化剂、油漆颜料和鞣剂等。