[拼音]:eryanghuagui
[外文]:silicon dioxide
化学式SiO2。自然界存在的二氧化硅叫做硅石,约占地壳总重量的12%。硅石常以石英、鳞石英和方石英三种变体出现。除晶体外,还有无定形(或微晶体)二氧化硅矿石,如蛋白石和硅藻土,它们都是含不定量结晶水的二氧化硅SiO2·nH2O。某些石英矿有特殊的名称,如大而透明的石英晶体叫水晶,含微量杂质而呈紫色的叫紫水晶,浅黄、金黄和褐色的叫烟水晶,黑色几乎不透明的叫墨晶。微晶体石英与其他物质混合的矿石有玛瑙和碧玉等。常见的砂子是含杂质的石英。
物理性质石英、鳞石英和方石英在高温和低温下有两种变体,它们的关系如下:
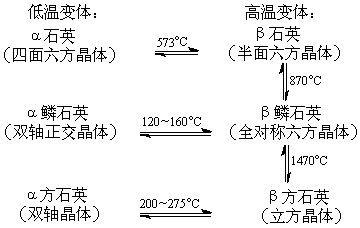
在所有变体的结构中,每个硅原子都同周围4个氧原子结合成SiO4四面体,而每个氧原子都被两个四面体所共用。由于这些四面体在空间的排布不同,使这些变体具有不同的无限三维结构,如石英具有一种螺旋状排布,所以有旋光异构体(见旋光异构)存在。
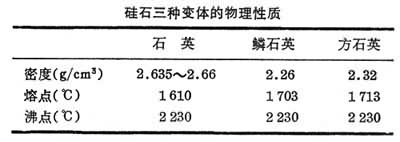
硅石的物理性质见表。晶态二氧化硅的硬度都很高,如石英的莫氏硬度为7;无定形二氧化硅硬度较低,其中较硬的蛋白石为5.5~6.5。
 化学性质
化学性质
二氧化硅的化学性质不活泼。在高温下氢不能还原二氧化硅。除单质氟、氟化氢和氢氟酸以外,二氧化硅与其他卤素、卤化氢和氢卤酸都不起作用。二氧化硅与硫酸、硝酸和高氯酸也不起作用。
在高温下,二氧化硅能被碳、镁或铝还原:
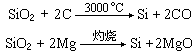
在微量水存在下,氟化氢与二氧化硅发生如下反应:
4HF+SiO2─→SiF4+2H2O
二氧化硅溶于氢氟酸,生成易溶于水的氟硅酸:
SiO2+6HF─→H2SiF6+2H2O
二氧化硅能溶于热的浓强碱溶液,也能溶于熔融的强碱或碳酸钠:
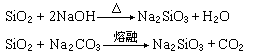 应用
应用
二氧化硅是制造水玻璃、耐火材料、普通玻璃、光学玻璃、导光纤维、石英玻璃仪器的原料,也是制造金刚砂 SiC及其他硅化合物的原料。具有压电性的单晶石英可制做超声波元件。硅藻土可做工业用吸附剂和保温、隔音材料。水晶可制作镜片或光学仪器,玛瑙和碧玉可做装饰宝石。