[拼音]:relixue hanshu jiben guanxishi
[外文]:fundamental equations of thermodynamic functions
对于封闭系统,将热力学第一定律与热力学第二定律相结合,可以得到如下一组关系式:
dU=TdS-pdV (1)
dH=TdS+Vdp (2)
dA=-SdT-pdV (3)
dG=-SdT+Vdp (4)
式中U为内能;H为焓;A为亥姆霍兹函数;G为吉布斯函数;S为熵;T为热力学温度;V为体积;p为压力。这一组关系式就称为封闭系统的热力学函数基本关系式。式(1)~(4)只适用于内部平衡且不做非体积功的封闭系统。
利用上述基本关系式的积分,可以求得一个封闭系统经历一个任意可逆过程后状态函数的变化。对于只由两个独立变量便可描述的封闭系统(即没有不可逆的化学变化和相变化的封闭系统),上述基本关系式实际上可看作状态函数U、H、A和G的全微分表达式。无论过程是否可逆,它们的积分都存在,且只由系统的始、终态决定。因此,对这样的系统,不可逆过程的状态函数的变化,也可由上述基本关系式积分求得。
利用封闭系统的热力学基本关系式,还可以推导出许多重要的关系式。例如,从式(1)~(4)可导出:
T=(дU/дS)V=(дH/дS)p (5)
p=-(дU/дV)S=-(дA/дV)T (6)
V=(дH/дp)S=(дG/дp)T (7)
S=-(дA/дT)V=-(дG/дT)p (8)
利用数学上的全微分性质,还可由式(1)~(4)导出:
(дT/дV)S=-(дp/дS)V (9)
(дT/дp)S=(дV/дS)p (10)
(дS/дV)T=(дp/дT)V (11)
(дS/дp)T=-(дV/дT)p (12)
式(9)~(12)称为麦克斯韦关系式组。利用此关系式,可把一些实验上难以测量的量〔如(дS/дp)T〕转化为易于测量的量〔如(дV/дT)p〕。
利用麦克斯韦关系式,可从式(1)和(2)导出:
(дU/дV)T=T(дp/дT)V-p (13)
(дH/дp)T=-T(дV/дT)p+V (14)
式(13)、(14)描述了系统的内能U和焓H随系统的体积和压力的变化关系,通常称为热力学状态方程。
对化学组成可变的均相系统,式(1)~(4)可改写为:
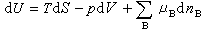 (15)
(15)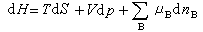 (16)
(16)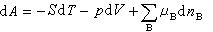 (17)
(17)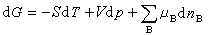 (18)
(18)
式(15)~(18)称为开放系统的热力学函数基本关系式。式中μB为系统中物质B的化学势;dnB为物质B的物质的量的微小变化值。
如果系统在变化过程中除体积功和化学功外还有其他功(如电、磁、表面功等),则热力学函数基本关系式的形式为
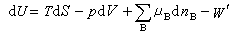 (19)
(19)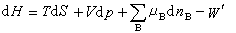 (20)
(20)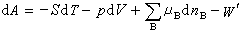 (21)
(21)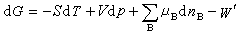 (22)
(22)
式中W ′为除体积功以外的其他功。