近年来随着工业生产的快速发展,能源和环境污染问题一直受到人们的普遍关注。对工业污染治理技术的要求不断提高,光催化技术在环境治理方面的研究也越来越多。利用太阳能源光催化降解污染物已成为研究的热点之一〔1, 2〕。半导体材料在光的照射下将光能转化为化学能,促进化合物的合成或使化合物降解从而实现光催化〔3〕。Mn2+是一种过渡金属离子,将其掺杂在半导体光催化材料中能显著提高材料的光电性质〔4〕。且含Mn半导体纳米材料作为一种典型的稀磁半导体,具有较大的直接禁带宽度及较好的磁光性能〔5〕。CdS是常见的光电半导体材料,在光吸收、光催化、光电转换等方面有较为广泛的应用〔6, 7〕。虽然过渡金属离子掺杂和半导体材料的研究取得了较好的进展,但是将二者很好地结合起来即过渡金属离子掺杂半导体材料的相关研究报道却不多。Libo Yu等〔8〕采用温和的水热法,以导电玻璃为衬底,在透明氟掺杂氧化锡上合成了一维二氧化钛纳米棒阵列,并将其应用在量子点敏化太阳能电池上。当太阳光照明度为0.1 W/cm2时,CdSe/Mn-CdS/二氧化钛太阳能电池的功率转换效率达到2.40%,其转换效率高于没有掺杂锰的CdSe/CdS/二氧化钛太阳能电池。Qizhao Wang等〔9〕研制了一种新型生物高聚物-Pd/CdS复合光催化剂,并在可见光照射下用该催化剂对Rh-B进行光催化降解,表现出很高的光催化活性。这种催化剂不仅能提高贵金属Pd的利用率,而且能提高对染料的降解效率;当Pd在该催化剂中的质量分数占0.5%时,其可见光催化活性最高。笔者所在课题组以Cd(CH3COO)2・2H2O、Mn(CH3COO)2・4H2O及Na2S・9H2O为原料,采用共沉淀方法合成了Mn/CdS光催化剂。当w(Mn)为0.50%时,Mn/CdS光催化降解甲基橙的降解率达84.7%。
1 实验部分
1.1 实验试剂
四水合乙酸锰,国药集团化学试剂有限公司;二水合乙酸镉,国药集团化学试剂有限公司;九水合硫化钠,上海纯亚化工科技发展有限公司;甲基橙,天津市大茂化学仪器供应站;以上试剂均为分析纯。
1.2 实验仪器
XD-3X射线衍射仪,北京普析通用仪器有限责任公司;CM200-FEG型高分辨透射电镜(加速电压 200 kV),Philips公司;XPA系列光化学反应仪,南京胥江机电厂;TGL-20M台式高速离心机,长沙平凡仪器仪表有限公司;TU-1901紫外-可见分光光度计,北京普析通用仪器有限责任公司;PLSSXE300/300UV氙灯模拟日光光灯,北京泊菲莱科技有限公司;722N可见分光光度计,上海元析仪器有限公司;ZJB400紫外截至镜片,杭州汇龙光电仪器厂。
1.3 Mn/CdS光催化剂的制备
将2.000 g Cd(CH3COO)2・2H2O和不同质量比例的Mn(CH3COO)2・4H2O放入烧杯中,用适量去离子水溶解,然后向其中缓慢滴加Na2S溶液并不停搅拌,可得到Mn质量分数不同的Mn/CdS沉淀。将该沉淀用去离子水反复洗涤,放在80 ℃真空干燥箱中干燥5 h即可。
1.4 紫外光下Mn/CdS光催化剂活性测定
准确称取Mn质量分数分别为0、0.25%、0.50%、1.00%、2.50%、5.00%的Mn/CdS光催化剂0.05 g置于6个石英管中,分别编号1、2、3、4、5、6;分别向其中加入40 mL的20 mg/L甲基橙溶液,再放入磁子。把石英管放入XPA系列光化学反应仪中,不断搅拌下暗反应30 min,取样离心,测其吸光度(A0);打开300 W高压汞灯,光照1 h,取样离心,测其吸光度(A1),计算降解率。绘制Mn/CdS光催化剂对甲基橙溶液的光催化降解曲线。
1.5 清除剂对Mn/CdS光催化剂活性的影响
准确称取5份Mn质量分数为0.50%的Mn/CdS光催化剂0.05 g,放入石英管中,并编号1、2、3、4、5,其中1号管不添加清除剂,其余4个管分别加入异丙醇0.003 8 mL、草酸铵0.004 g、对苯醌0.004 g、过氧化氢酶0.005 mL,然后再向5支石英管中加入40 mL 20 mg/L的甲基橙溶液,以下操作同1.4。根据所得降解率绘制不同清除剂存在下的光催化降解曲线。
2 实验结果与讨论
2.1 Mn质量分数对Mn/CdS光催化剂活性的影响
不同Mn质量分数下光催化剂降解甲基橙溶液的紫外光催化活性如图 1所示。
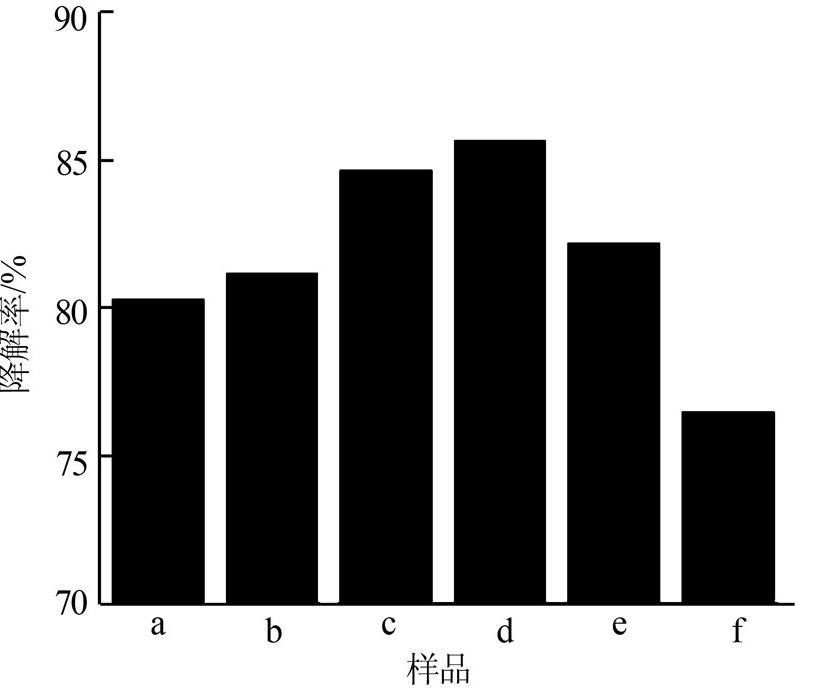
注:a―0,b―0.25%,c―0.5%,d―1.0%,e―2.5%,f―5.0%。
图 1 不同Mn质量分数的Mn/CdS
从图 1可知:Mn/CdS光催化剂对甲基橙的降解率随着Mn质量分数的增加而增大,在Mn质量分数为0.5%、1.0%时达到最高,降解率分别为84.7%、85.7%,此后其光催化降解率随Mn质量分数的增加而降低,最低降解率为76.5%。原因是Mn含量较低时,Mn镶嵌在CdS固体的表面,可以很好地吸附大量有机污染物,使催化效率增加;当Mn含量过高时,CdS固体表面达到饱和,多余的Mn颗粒就会悬浮在溶液中,部分光被反射及折射掉,使光源利用率降低,从而导致催化效率降低〔10, 11〕。
2.2 清除剂对Mn/CdS光催化降解甲基橙溶液的影响
清除剂会与光催化反应生成的活性基团发生反应,并降低光催化剂的活性。为验证反应生成的活性物种类型,投加不同的清除剂,考察其对光催化剂(Mn质量分数分别为0、0.5%)降解甲基橙溶液的影响,结果见图 2、图 3。
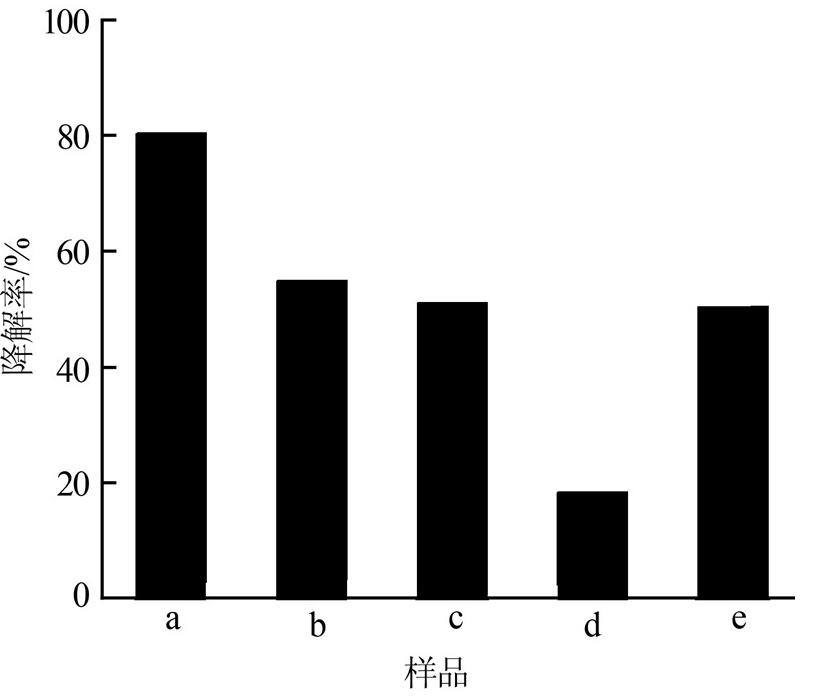
注:a―不加清除剂,b―异丙醇,c―草酸铵,d―对苯醌,e―过氧化氢。
图 2 清除剂对CdS光催化降解甲基橙溶液的影响 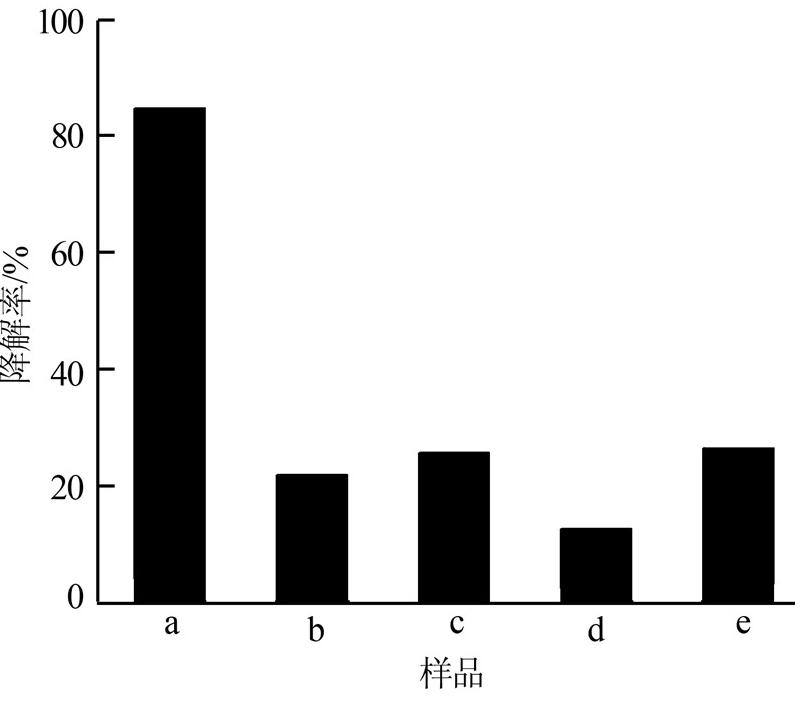
由图 2、图 3可知:(1)加入不同种类的清除剂后,Mn/CdS光催化剂对甲基橙溶液的光催化降解率下降;(2)加入对苯醌清除剂后,甲基橙溶液的光催化降解率显著下降,当w(Mn)分别为0、0.5%时,Mn/CdS光催化降解率分别为18.3%、12.5%。据相关文献报道,光催化降解过程中起主要作用的离子应该是・O2-,加入对苯醌后,它可以与溶液中的・O2-作用,从而降低溶液中的・O2-浓度,使催化降解效率大大降低〔12, 13〕。
2.3 Mn/CdS光催化剂的XRD
图 4为Mn/CdS光催化剂的XRD谱图。
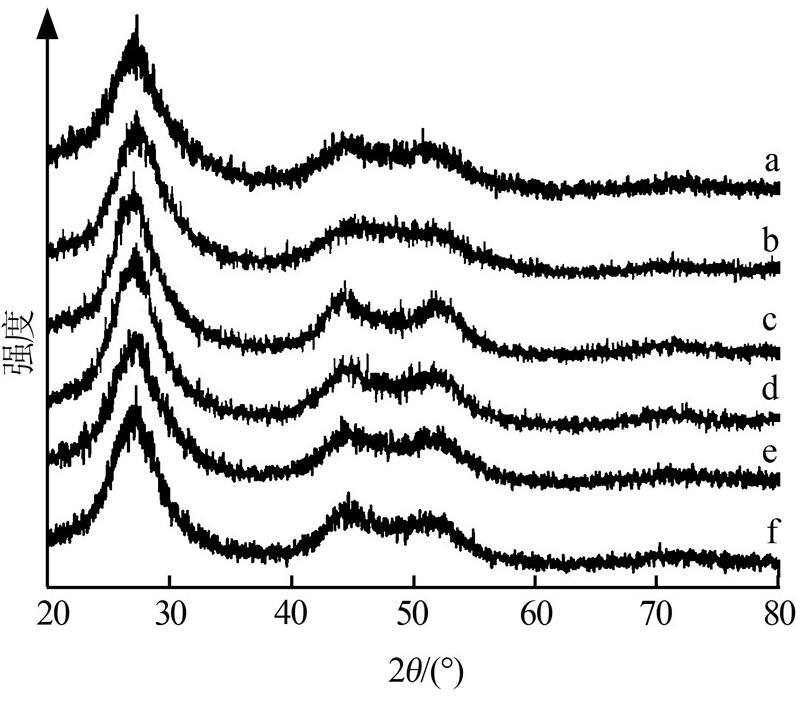
注:a―0,b―0.25%,c―0.5%,d―1.0%,e―2.5%,f―5.0%。
图 4 不同Mn质量分数光催化剂的XRD谱图
从图 4可以看出,2θ为27.2°处有1个吸收强度最强的峰,对应晶面为(111),为CdS的特征峰〔14〕。因此可以推测出笔者采用共沉淀方法制得的样品中存在CdS;查阅相关文献得知,Mn/CdS光催化剂的XRD谱图中还应存在1个Mn的吸收峰,通过分析认为可能是Mn含量过低,Mn的吸收峰太弱,被其他的峰所掩盖。
2.4 Mn/CdS光催化剂的HRTEM谱图
HRTEM可表征催化剂的形貌特征,其中晶面间距越小,催化剂活性越高。CdS、Mn/CdS光催化剂的HRTEM谱图如图 5、图 6所示。
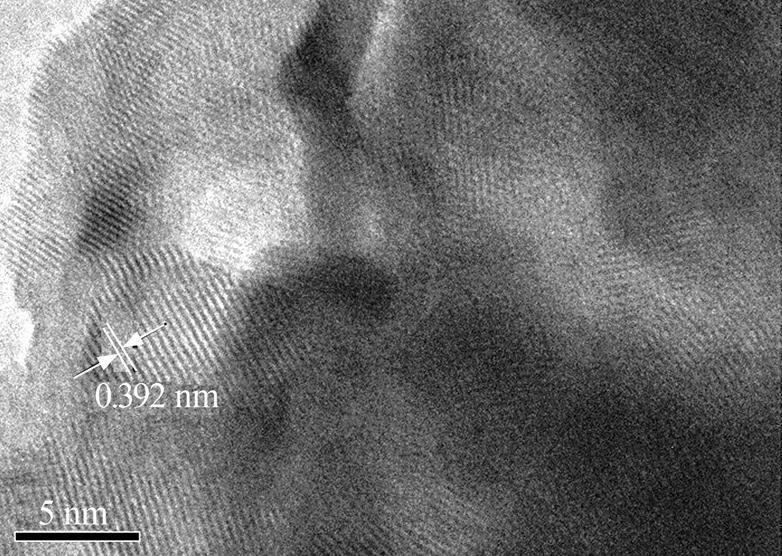
图 5 CdS光催化剂的HRTEM谱图
对比图 5、图 6可以看出Mn/CdS光催化剂的Mn质量分数为0.5%时,晶面间距为0.357 nm,当Mn质量分数为0时,晶面间距为0.392 nm,晶面间距变小,晶体半径同样会变小,即Mn质量分数为0.5%时得到的晶体半径小,且晶体的凝聚度低。。
3 结论
以Cd(CH3COO)2・2H2O、Mn(CH3COO)2・4H2O及Na2S・9H2O为原料,采用共沉淀法合成了Mn/CdS光催化剂。以甲基橙为光催化反应的模型化合物,评估了Mn/CdS光催化剂的紫外光催化活性,并探讨了清除剂对Mn/CdS紫外光催化活性的影响。当w(Mn)为0.50%时,Mn/CdS对甲基橙的降解率最高为84.7%。













