[拼音]:silühuagui
[外文]:silicon tetrachloride
化学式SiCl4。无色易挥发液体;熔点-68℃,沸点57.6℃,密度1.48克/厘米3。四氯化硅在湿空气中强烈发烟,有强吸湿性和水解性,能溶于苯、乙醚和四氯化碳。
四氯化硅遇水强烈水解,生成硅酸凝胶:
SiCl4+4H2O─→H4SiO4+4HCl
四氯化硅与金属氧化物在加热下作用,生成金属氯化物和二氧化硅,例如:
3SiCl4+2Al2O3─→4AlCl3+3SiO2
四氯化硅也能与非金属氧化物作用,使氧被氯取代。例如,SiCl4可使P2O5变为POCl3,也可使SO3变为S2O5Cl2。四氯化硅与氨作用生成Si(NH2)4,将产物加热时可得一系列硅的氮化物:
SiCl4+8NH3─→Si(NH2)4+4NH4Cl
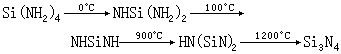
四氯化硅在加热下可被金属钠或氢气还原成单质硅:
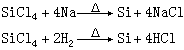
四氯化硅与单质硅作用,生成Si2Cl6:
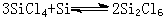
在氯气中加热二氧化硅和碳,可得四氯化硅:
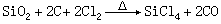
四氯化硅是制备有机硅化合物的原料;也常用作易被提纯的中间原料,用于生产纯硅和单晶硅。