[拼音]:rongye pH de dianwei cedingfa
[外文]:potentiometric determination of pH of solution
当一个 pH 指示电极(如玻璃电极)和一个参比电极插入被测溶液时,参比电极与指示电极间的电位差V决定于溶液的pH。25℃时两者的关系为:
V=b+0.0592pH
式中 b为常数。利用pH计(见彩图)

测定溶液的pH时,要先用已知pH值的缓冲溶液校准仪器,这时的电位差VS为:
VS=b+0.0592pHS
然后再测定未知溶液的pH:
Vu=b+0.0592pH
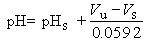
式中Vu为用未知溶液时产生的电位差, 此式表明溶液的pH是以标准缓冲溶液的pHS和电位差VS计算的。这是实际测定中使用的pH的定义。
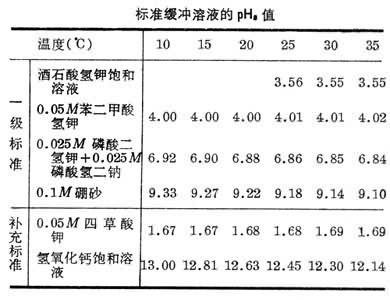
标准缓冲溶液的pHS值的测定分三步:
(1)在被测的缓冲溶液中加入少许一定量的可溶性氯化物,在溶液中插入氢电极和银│氯化银电极,然后测定电池的电动势E:
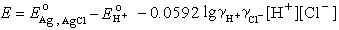
式中γ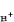 和γ扲 分别为 H+和 Cl-的活度系数,
和γ扲 分别为 H+和 Cl-的活度系数,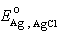 和
和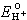 为标准电极电位,令PWH为:
为标准电极电位,令PWH为:
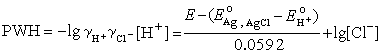
式中E、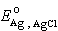 、
、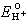 、[Cl-]都可测定,所以PWH即可求得。
、[Cl-]都可测定,所以PWH即可求得。
(2)当[Cl-]小于0.015Μ时,PWH对[Cl-]作图, 得一直线。在不同的[Cl-]值时求出PWH值,并以PWH值对[Cl-]作图,求出[Cl-]=0时的PWH值(以PWH0表示)则得:
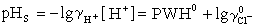
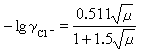
式中μ为离子强度。由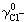 就可以求出pHS。
就可以求出pHS。
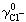 ,在25℃时:
,在25℃时: