[拼音]:liu xunhuan
[外文]:sulfur cycle
自然界硫循环的基本过程是:陆地和海洋中的硫通过生物分解、火山爆发等进入大气;大气中的硫通过降水和沉降、表面吸收等作用,回到陆地和海洋;地表径流又带着硫进入河流,输往海洋,并沉积于海底。在人类开采和利用含硫的矿物燃料和金属矿石的过程中,硫被氧化成为二氧化硫(SO2)和还原成为硫化氢(H2S)进入大气。硫还随着酸性矿水的排放而进入水体或土壤。自然界中硫的分布、硫的流动和交换见表1和表2。
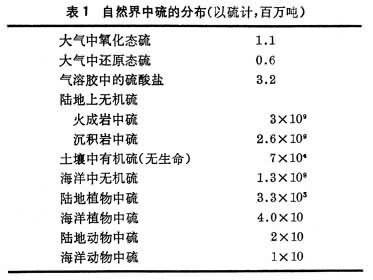
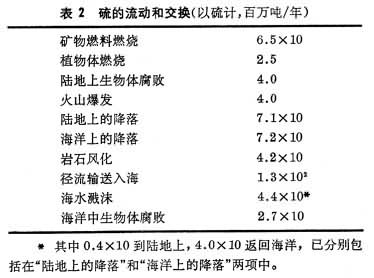
自然界的硫循环
陆上火山爆发,使地壳和岩浆中的硫以H2S、硫酸盐和SO2的形式排入大气。海底火山爆发排出的硫,一部分溶于海水,一部分以气态硫化物逸入大气。陆地和海洋中的一些有机物质由于微生物分解作用,向大气释放H2S,其排放量随季节而异,温热季节高于寒冷季节。海洋波浪飞溅使硫以硫酸盐气溶胶形式进入大气。
陆地植物可从大气中吸收SO2。陆地和海洋植物从土壤和水中吸收硫。吸收的硫构成植物本身的机体。植物残体经微生物分解,硫成为H2S逸入大气。
大气中的SO2和H2S经氧化作用形成硫酸根(SO厈),随降水降落到陆地和海洋。SO2和SO厈还可由于自然沉降或碰撞而被土壤和植物或海水所吸收。由陆地排入大气的SO2和SO厈可迁移到海洋上空,沉降入海洋。同样,海浪飞溅出来的SO厈也可迁移沉降到陆地上。陆地岩石风化释放出的硫可经河流输送入海洋。水体中硫酸盐的还原是由各种硫酸盐还原菌进行反硫化过程完成的。在缺氧条件下,硫酸盐作为受氢体而转化为H2S。
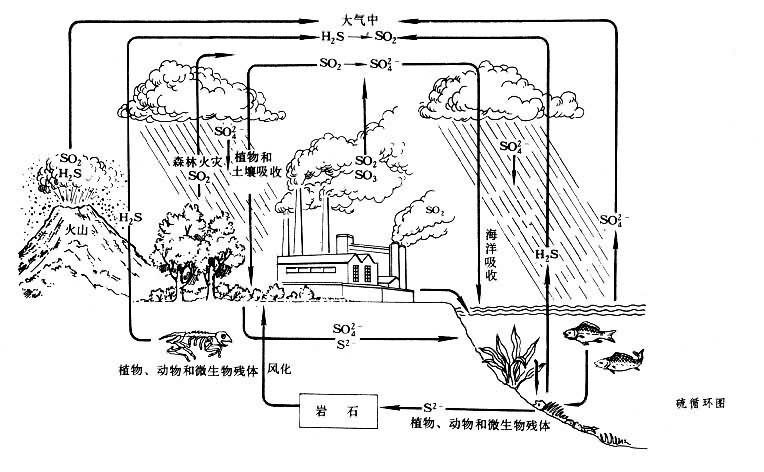
人类活动的干预
人类燃烧含硫矿物燃料和柴草,冶炼含硫矿石,释放大量的SO2。石油炼制释放的H2S在大气中很快氧化为SO2。这些活动使城市和工矿区的局部地区大气中 SO2浓度大为升高,对人和动植物有伤害作用(见二氧化硫污染对健康的影响)。SO2在大气中氧化成为SO厈,是形成酸雨和降低能见度的主要原因。
- 参考书目
- J.Q.Nriagu,Sulfur in the Environment,JohnWilley &Sons,New York,1978.