[拼音]:wending changshu
[外文]:stability constant
在溶液中配位化合物(简称配合物)的形成反应的平衡常数。稳定常数是衡量配合物在溶液中稳定性的尺度,其值越大越稳定。在水溶液中,配合物的形成是水合金属离子M(H2O)n中内层的水分子被配体L取代的反应(离子所带电荷从略):
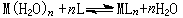
以上反应的平衡常数为:
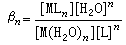 (1)
(1)
式中方括号内表示各质点的平衡浓度;βn为化学计量积累稳定常数。通常取代反应是逐级进行的,逐级稳定常数Kn为:
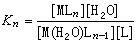 (2)
(2)
显然,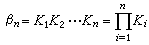 。水的浓度可认为是恒定的,所以式(1)和(2)中[H2O]为常数,可并入左边,而右边不必写出。若平衡浓度以活度a代替,则相应的平衡常数称为热力学稳定常数Tβn(或TKn):
。水的浓度可认为是恒定的,所以式(1)和(2)中[H2O]为常数,可并入左边,而右边不必写出。若平衡浓度以活度a代替,则相应的平衡常数称为热力学稳定常数Tβn(或TKn):
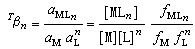
其中活度系数 f近似地仅与离子强度有关,在测定化学计量稳定常数时,常在溶液中加入惰性盐以维持离子强度不变。
配合物在溶液中形成时,常引起某一种物理化学性质的改变。测定稳定常数的方法就是以此为基础。大致有以下几种:
电位法以研究溶液中离子与电极的相互作用为基础,来测定金属离子或配体的活度。电位法所测的数据精确,适用于单核、混合和多核配合物的研究,应用范围最广泛。用电位法测定稳定常数时,要求电极反应必须是可逆的。使用的电极主要有金属或金属汞齐电极、氧化还原电极和离子选择性电极三种。金属汞齐电极使用较广,适用于Cu2+、Zn2+、Cd2+、In3+、Tl+、Sn2+、Pb2+、Bi3+等金属配合物的研究。用玻璃电极测定稳定常数,称为pH电位法(见溶液pH的电位测定法),可以测量配合物形成时溶液pH的变化,再用所得结果计算稳定常数。用pH电位法测定稳定常数时,要求配合物在溶液中有足够的溶解度,在反应过程中无沉淀生成,配体的碱度要适中。该法在测定螯合物(见螯合作用)的稳定常数时特别有效。各种离子选择性电极是近年来出现的新方法,目前品种有限,可测的离子不多。
极谱法也是以研究溶液中离子与电极的相互作用为基础的方法。根据加入配体后金属离子的半波电位的改变来计算稳定常数,在金属离子可逆还原条件下,能得到单核和混合配合物的稳定常数。该法数据准确可靠,灵敏度高,特别适用于浓度和稳定性较低的配合物。对某些不可逆还原的金属离子,可采用竞争法或利用扩散电流随配体浓度改变的关系来计算(见极谱法和伏安法)。
分光光度法当配合物的吸收光谱与金属离子有所不同,且溶液在某一波长的光密度与组成的关系符合比尔定律时,稳定常数可通过计算求得。其优点是迅速可靠,适用于低浓度(10-4~10-5)的配合物,溶剂选择的范围比电位法广,但处理数据的未知数比电位法多,对较复杂体系的计算有一定困难(见紫外-可见分光光度法)。
萃取法和离子交换法均以金属配合物的异相分配为基础,通过测定分配比来测定稳定常数。这两种方法的精确度不如电位法,但不低于分光光度法,特别是当金属离子浓度很低时,可采用放射性手段来测定,这是其独特的优点。萃取法(见溶剂萃取)适用于研究螯合物,不适用于稳定性较低的配合物。离子交换法适用于微量的或含放射性金属离子的配合物的研究,但手续较麻烦,数据不够精确。
量热滴定法又称测温滴定法,是20世纪60年代发展起来的新方法,根据配位反应的热效应来确定组成和稳定常数。该法用热敏电阻感温,用电子计算机计算,通过一次滴定可同时求得配位反应热焓 ΔH和稳定常数值,能直接而准确地获得ΔH、ΔG(吉布斯函数)和ΔS(熵)值。此法应用范围广,反应条件适应性强,对高酸度、高碱度和非水体系均可适用,特别适用于pH值恒定的生物缓冲体系。但不如pH电位法和分光光度法有高度的专一性。因其计算复杂,校正项多,用于复杂体系时有一定的困难。
其他方法均以配位过程中某一物理量的改变为基础,如核磁共振法(见核磁共振谱)以化学位移或偶合常数为基础,顺磁共振法(见电子自旋共振)除根据偶合常数外,还可根据谱线宽度(弛豫时间)、谱线强度(自旋浓度)及朗德因子值来计算。这些方法皆有局限性,使用范围不广。
- 参考书目
- F. J. C. Rossotti and H. S. Rossotti,The Determination of Stability Constants,McGraw-Hill,New York,1961.
- F.R.Hartley,C.Burgess and R. Alcock,Solution Equi-librium, John Wiley & Sons, New York,1980.