[拼音]:zhonghe
[外文]:neutralization
酸和碱的相互作用。一般认为酸与碱反应,生成盐和水,例如:
NaOH+HCl─→NaCl+H2O
中和的实质是:
H++OH-─→H2O ΔH°=-57.32kJ/mol
阿伦尼乌斯电离理论认为:弱酸(碱)在水溶液中只有部分电离,它与强碱(酸)的中和热低于57.32千焦/摩尔。
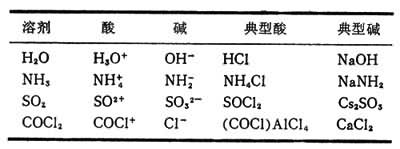
严格说来,“中和生成盐和水”的说法不妥,因为上例中的Na+和Cl-并未参加反应。又如按照路易斯酸碱理论(见酸碱理论),在液氨溶液中NH嬃(酸)与NH娛(碱)作用生成的是NH3而不是H2O:
NH嬃+NH娛─→2NH3
所以“生成水”,只是在一定条件下中和反应的一种结果,而不是唯一的结果。然而,生成溶剂是大多数中和反应的共同特点,如: