[拼音]:lühua yejin
[外文]:chlorine metallurgy
添加氯化剂(Cl2、NaCl、CaCl2等)使欲提取的金属转变成氯化物,为制取纯金属作准备的冶金方法。金属和金属的氧化物、硫化物或其他化合物在一定条件下大都能与化学活性很强的氯反应,生成金属氯化物。金属氯化物与该金属的其他化合物相比,具有熔点低、挥发性高、较易被还原、常温下易溶于水及其他溶剂等特点,并且各种金属氯化物的生成难易和性质上存在着明显的差异。在冶金中,常常利用上述特性,借助氯化冶金有效地实现金属的分离、富集、提取与精炼等目的。早在16世纪中叶就发现含金、银的矿石在浸取(浸出)过程中,加入一定量的食盐,可以提高金属的回收率。18世纪出现了氯化焙烧-浸取法处理贵金属矿石,效果更好。到19世纪中期,此法扩大应用于处理低品位铜矿石。这是氯化冶金应用的一个重要发展。20世纪20年代,氯化冶金除了应用于镁的提取之外,还以氯化离析法用于提取有色重金属(主要是铜)。50年代以来,氯化冶金广泛用于稀有金属冶金中。
类型
氯化焙烧视原料性质和下一步处理方法的不同,有中温氯化焙烧和高温氯化焙烧:前者是使被提取的金属氯化物在不挥发的条件下进行,所产生的氯化物可用水或其他溶剂浸取而与脉石分离;后者是在被提取的金属氯化物能挥发的温度下进行,所形成的氯化物呈蒸气状态挥发,与脉石分离,然后冷凝回收。此法用于菱镁矿(MgCO3)和金红石(TiO2)的氯化,以生产镁和钛,亦用于处理黄铁矿烧渣,综合回收铜、铅、锌、金、银等。
氯化离析在矿石中加入适量的碳质还原剂(煤或焦炭)和氯化剂,在弱还原性气氛中加热,使有价金属成氯化物挥发,同时氯化物又在炭粒表面被还原为金属的过程(见离析)。此法已用于处理某些低品位或难选氧化矿(如氧化铜矿)。
氯化熔炼使要提取的金属氯化物呈熔融状态产出的过程。例如通氯气于氧化镁和碳质还原剂的混合物中,使镁变成液态氯化镁。
氯化精炼例如,液态粗铝中所含的杂质,如钠、钙和气体氢,或液态铅中所含的锌,都可用氯气进行精炼。氯化精炼的工业应用较少。
氯化浸取在水溶液中进行的氯化过程,即湿法氯化,包括盐酸浸取、氯盐浸取、氯气浸取和电氯浸取。
主要内容
可概括为:各种金属元素或化合物的氯化,氯化物的分离和还原。
金属氧化物的氯化反应式为:
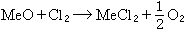 (1)
(1)
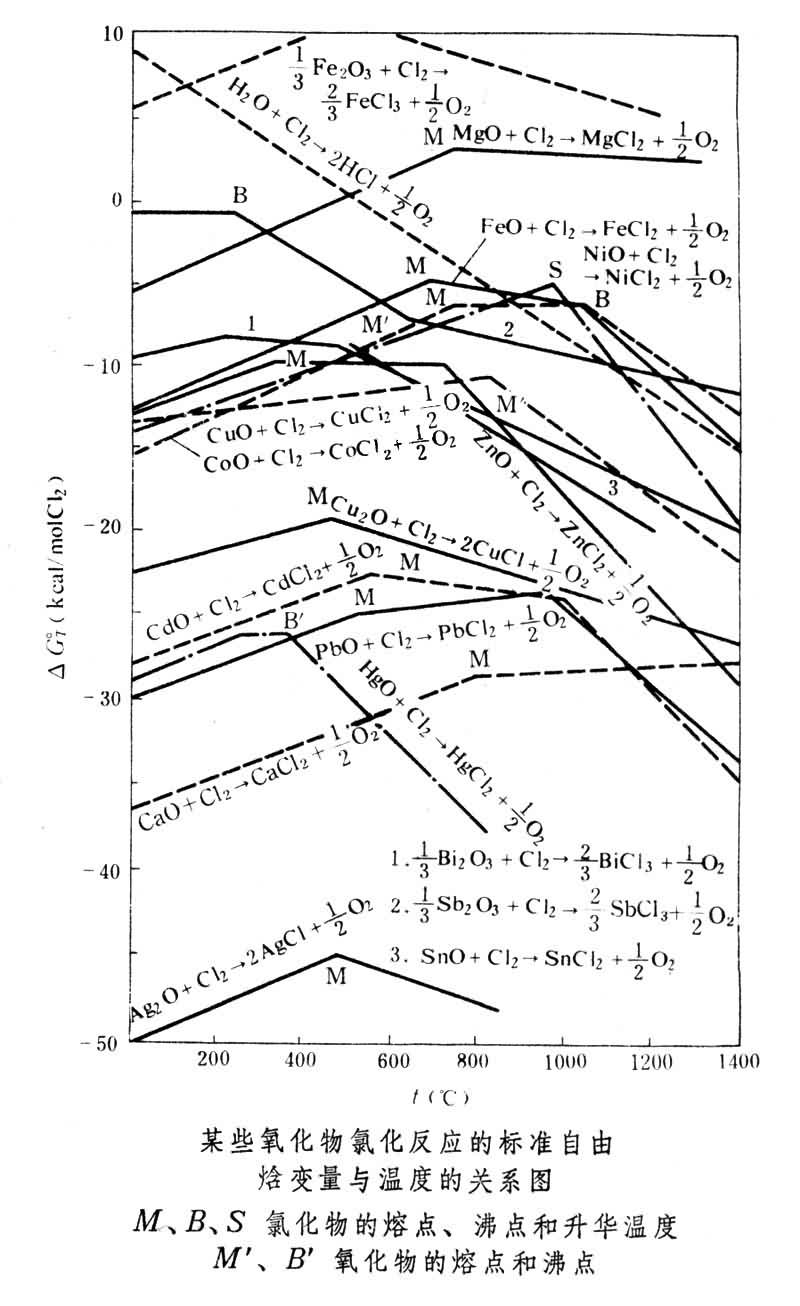
式中Me表示二价金属,各氧化物氯化反应的标准自由焓变量与温度的关系见图。由图可见,银、镉、铜、钴等金属的氧化物都能被氯气所氯化,只是氯化的难易程度不同。实际上,氯化过程并非都在标准状态下进行,所以氯化反应能否进行,用自由焓变量来衡量更为确切。假定MeCl2和MeO为纯凝聚相,活度均为1,此时反应式(1)的自由焓变量可表示为:
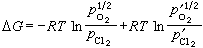
式中R为气体常数,T为绝对温度,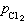 、
、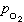 为Cl2和O2的平衡分压,
为Cl2和O2的平衡分压,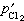 、
、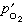 为Cl2和O2的实际分压。显然,要使反应向生成氯化物方向进行,必须保持:
为Cl2和O2的实际分压。显然,要使反应向生成氯化物方向进行,必须保持:
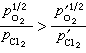
由此可见,可以通过改变反应温度和气相组成来选择要提取的金属氧化物优先氯化的条件。
显然,气相中氧分压降低可大大促进氧化物的氯化。常用的还原剂为碳(焦炭、煤和木炭)和一氧化碳。在此情况下,氯化反应按下列各式进行:MeO+Cl2+C─→MeCl2+CO (2)
2MeO+2Cl2+C─→2MeCl2+CO2 (3)
MeO+Cl2+CO─→MeCl2+CO2 (4)
C或CO与氧化物中的氧结合,可使氯化反应的自由焓变化值减小。例如,1000℃时二氧化钛的氯化:
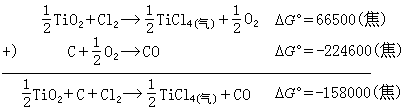 金属热还原法还原氯化物
金属热还原法还原氯化物
例如用镁还原四氯化钛生产海绵钛:
TiCl4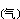 +2Mg
+2Mg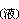 →Ti
→Ti +2MgCl2
+2MgCl2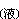 (5)
(5)
此反应在714~1000℃的自由焓变量负值很大,TiCl4极易被镁还原为金属钛。
特点
氯化冶金具有以下优点:
(1)对原料的适应性强,可处理各种不同类型的原料,甚至液态粗金属;
(2)作业温度比其他火法冶金过程低;
(3)分离效率高,综合利用好。在高品位矿石资源逐渐枯竭的情况下,对储量很大的低品位、成分复杂难选的贫矿来说,氯化冶金将发挥它的作用。但是尚有三个问题待解决:
(1)提高氯化冶金的经济效益,其中提高氯化剂的利用效率和氯化剂的再生返回利用是关键性问题;
(2)继续解决氯化冶金设备的防腐蚀;
(3)环境保护。