�ҹ�������Ⱦ�����ŷ�Ũ�����ƣ����������һ����Ⱦ���һ��Ļ�ѧ������ˮ�к�Ni2+�ߴX�ٵ���ǧmg/L������о���ѧ������ˮ�Ĵ�������������Ҫ���塣Ŀǰ���õĺ�����ˮ�Ĵ�����������ѧ�����������ӽ��������������������������кͷ�����ⷨ�ȡ��������������ǻ�ѧ�������е�һ�֡���Ŀǰ�������й����������巨������Ũ�Ȼ�ѧ������ˮ��Ӧ���о���δ��������
����ൺij���ӳ������ĸ�Ũ�Ȼ�ѧ������ˮ�����߲��������巨���������Ԥ�����о���������ʵ��͵������Ż�ʵ��2 ���濼����n��Fe2+����n��Fe3+����m��FeSO4��7H2O����m��Ni2+����pH����Ӧ�¶Ⱥͽ���ʱ���Ni2+ȥ���ʵ�Ӱ�죬����Ϊ�����巨������Ũ�Ȼ�ѧ������ˮ�ṩһ�������۲ο���
1 ʵ�鲿��
1.1 ��ˮ����Դ����������
ʵ���÷�ˮ����ɽ���ൺij���ӳ���ѧ������ˮ�������ŷ���Ϊ700��800 L����ˮ�е�����Ҫ������������ʽ���ڡ���ˮˮ�����£�pH=4.7��Ni2+Ϊ4 212.5 mg/L��COD Ϊ3.66��104 mg/L��ɫ��Ϊ1 000������ˮ��ɫ������ɫ��
1.2 ��Ҫ�������Լ�
������pHS-3C ������pH �ƣ�ALC-1100.2 ��Acculab ������ƽ��HH-2 �����Ժ���ˮԡ����TAS-986 �ͻ���ԭ�����շֹ��ȼƣ�JJ-1 ��ʱ�綯��������
�Լ���NaOH ��AR ������FeCl3��6H2O ��AR ������FeSO4��7H2O ��AR ������HNO3��AR ������ʵ����ˮ��Ϊ����ˮ��
1.3 ����·��
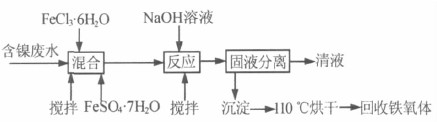
ʵ�鹤��������ͼ1 ��ʾ��
|
|
ͼ1 ��������
1.4 ʵ�鷽��
ȡ100 mL ��ѧ������ˮ��250 mL �ձ��У�Ͷ��һ������FeSO4��7H2O �����FeCl3��6H2O ���壬���裬�����ܽ�����164 g/L ��NaOH ��Һ������ˮ��pH����pH �ƲⶨpH��Ȼ����������һ���¶ȵĺ���ˮԡ���С����ڴ�ʱ��δ��ȫ��Ӧ����Ҫͬʱʹ����е�����豸����Һ���н��裬ת�ٿ�����500 r/min������һ��ʱ����á�1 h ����ù��˵ķ������й�Һ���롣����ԭ�����շֹ��ȷ��ⶨ��Һ�е������Ӻ��������ڹ�Һ����ķ�Ӧ������������ˮ������ϴ���Գ�ȥ�����е��������Ȼ����110 ���º�ɣ��ô���ȷ�������ǿ����
1.5 ��������
Ni2+����ԭ�����շֹ��ȷ��ⶨ��pH ��pH�����ƣ�ɫ�Ȳ���ϡ�ͱ������ⶨ���¶��ɺ���ˮԡ�����ƣ��γ�������Ĵ���ǿ���ɴ���ȷ����
2 ���������
2.1 ����ʵ����
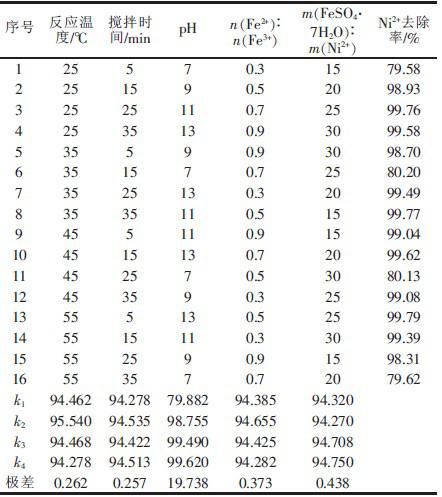
�����巨ȥ��Ni2+����ҪӰ�������з�Ӧ�¶ȡ�����ʱ�䡢pH��n ��Fe2+���� n��Fe3+����m��FeSO4��7H2O����m��Ni2+�������ȷ������L16��45������ʵ�飬��Ni2+ȥ����Ϊ����ָ�ꡣʵ��������1��
ͨ����������ó���pH ������Ҫ��Ӱ�����أ�����4 �����ص�Ӱ����Խ�С���������á�����ԭ��ˮ��Ni2+�����ܸߣ���Ӧ�������仯����ʹȥ��������С����ˮNi2+����Ҳ������ʮmg/L ���ҡ����Ϊ�˴ﵽ��Ѵ���Ч������Ҫ��pH �����������ؽ��е������Ż�ʵ�飬��ȷ����ѷ�Ӧ������
2.2 �������Ż�ʵ����
2.2.1 pH ��Ӱ��
pH ���ؽ����ij������ŷdz���Ҫ��Ӱ�죬������Һ��OH-����������������ķ�Ӧ�������Һ��pH ֱ��Ӱ�쵽��ˮ�е�Ni2+Ũ�ȡ���164 g/L NaOH��Һ��ΪpH ���ڼ�����m��FeSO4��7H2O����m��Ni2+��=19����Ӧ�¶�Ϊ30 �棬n��Fe2+����n��Fe3+��=0.6������ʱ��Ϊ15 min �������£�����pH ��Ni2+ȥ���ʵ�Ӱ�죬�����ͼ2��
��1 ����ʵ����
|
|
��ͼ2 ���Կ�������Ӧ��ϵ��pH ��Ni2+ȥ�����кܴ��Ӱ�졣����pH ������Ni2+ȥ����Ҳ��֮�������ǵ�pH ���ߣ�����ԭ������������һᵼ�³�ˮpH ���ߣ����ȷ����ѳ�ʼpH Ϊ10��11��������ȷ����ˮpH ��8.5��9.5 ֮�䡣���⣬��ʵ���л����֣���pH��9.5 ʱ�����ɵij������Ϊ�ֻ�ɫ���ػ�ɫ���������࣬û�д��ԣ��ҿ���ϸС����Һ�������ѣ�������pH �������˺�ɫ��������Һ�ֲ����ԣ�����Ϊ����״�ߴ��������塣��������Fe��OH��3���ɵ�pH Ϊ2.0 ���ң�Fe ��OH��2���ɵ�pH Ϊ5.5 ���ҡ�3���������Ի�ѧ������ˮ�м���Fe2+��Fe3+����������Fe��OH��3����������pH ������������Fe��OH��2��������pH ����6.5 ʱ���ſ�ʼ����Ni��OH��2������ͬʱ����Щ������Ni2+�����������ã�ʹ֮һ����������Ǵ�ʱ�ij��������������塣�������ڼ����Fe3+��Fe2+�࣬������ɵij������ػ�ɫ������pH��9.5 ʱ�����ֽ��������������С��Ni��OH��2�ij�����ǿ������Fe��OH��2��Fe��OH��3�γ���������������Ӧʱ���ӳ���ת����⾧ʯ�ͺ�ɫ�����壬������Ϊ��ɫ��3����
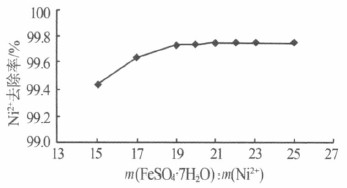
2.2.2 m��FeSO4��7H2O����m��Ni2+����Ӱ������Ӧ�����У�Ni2+����Fe2+����������������λ������NiFe2O4���������塣ʵ�鿼������pH=10.5��n��Fe2+����n��Fe3+��=0.6����Ӧ�¶�Ϊ30 �棬����ʱ��Ϊ15 min �������£���ͬm��FeSO4��7H2O����m��Ni2+����Ni2+ȥ���ʵ�Ӱ�죬�����ͼ3��
|
|
ͼ3 m��FeSO4��7H2O����m��Ni2+����Ni2+ȥ���ʵ�Ӱ��
��ͼ3 ���Կ���������Ͷ�ϱȵ�����ˮ��Ni2+ȥ���������ߡ���Ͷ�ϱ�Ϊ19 ʱ��Ni2+ȥ���ʴﵽ99.66%����������Ͷ�ϱȣ�ȥ���ʱ仯�����ۺϿ��ǣ�ѡȡ���Ͷ�ϱ�Ϊ21��ʵ���л����֣�����Ͷ�ϱȵ������γɵij�����ɫ�����ػ�ɫ��Ϊ��ɫ������Խ��Խϸ������һ���Ĵ��ԣ�˵������Ҫ�ɷ�Ϊ�����塣�ڴ��������У�ʵ������Ͷ����������Ͷ����������ԭ�����������ڷ�Ӧ�������в���Fe2+���������������ɵIJ���Fe��OH��2���������뵽������ķ�Ӧ�У������Գ�������ʽ�����������ҪͶ���㹻��Fe2+��ͨ�����ɴ����ij�������ʹNi2+��ȫ��Ӧ����˶��ڲ�ͬ�ĺ�����Ʒ�ˮ��Ͷ�ϱ�Ҳ��ͬ���辭ʵ��ȷ����
2.2.3 n��Fe2+����n��Fe3+����Ӱ��
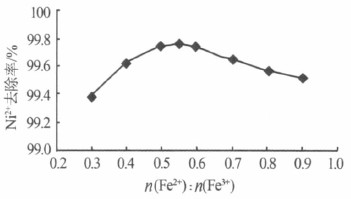
����������Fe2+��Fe3+��һ�������ʵ����ȴ��ڣ�������ֵΪ0.5����������ʵ�ʷ�Ӧ�У�����Fe2+�ᱻ�����Լ���ģ�����ѱ�ֵ����ݷ�ˮˮ�ʾ�ʵ�����ȷ����ʵ�鿼������pH=10.5��m��FeSO4��7H2O����m��Ni2+��=21����Ӧ�¶�Ϊ30 �棬����ʱ��Ϊ15min �������£���ͬn��Fe2+����n��Fe3+����Ni2+ȥ���ʵ�Ӱ�죬�����ͼ4����
��ͼ4 ��֪��n��Fe2+����n��Fe3+����0.4��0.5 ֮����һ��ֵ������ֵ̫С����Fe2+����̫��ʱ�����������㹻��Fe��OH��2����������������������NiFe2O4����Ҫ�����Ni2+��ȥ���ʵ͡��������Fe3+�ļ��룬�����ɴ�����Fe��OH��3������������Fe��OH��2��Ni��OH��2��Ӱ�췴Ӧ�Ľ��С����⣬����Fe2+���ױ������Լ�������ĵ�ԭ��ʵ����ѱ�ֵ�������ֵƫ��һ�㣬���ѡ�����n��Fe2+����n��Fe3+��Ϊ0.55��
|
|
ͼ4 n��Fe2+����n��Fe3+����Ni2+ȥ���ʵ�Ӱ��
2.2.4��Ӧ�¶ȵ�Ӱ��
��n ��Fe2 + ����n ��Fe3 + �� =0.55��m ��FeSO4��7H2O����m��Ni2+��=21��pH=10.5������ʱ��Ϊ15 min �������£����첻ͬ�¶���Ni2+��ȥ���ʣ������ͼ5��
|
|
ͼ5 ��Ӧ�¶ȶ�Ni2+ȥ���ʵ�Ӱ��
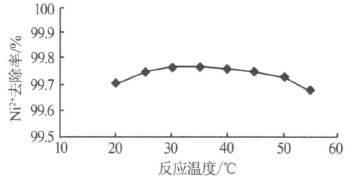
��ͼ5 ��֪����ʼʱNi2+��ȥ���������¶ȵ����߶����ߣ�����ȥ���ʻ������ͣ��������Ͽ����仯��������ԭ����Ҫ����Ϊ���¶ȹ���ʱ���ؽ��������˶��ٶ�������Ӧ�ٶ���������������������ɡ����¶ȹ���ʱ��Fe2+�����ױ����������ҽϸߵ��¶���������������������ƻ���Ҳ����������������ɡ�4��������ʵ���������ǵ����������Ӽ����豸��ʹͶ������ȷ��30 ��Ϊ��ѷ�Ӧ�¶ȡ�
2.2.5����ʱ���Ӱ��
��pH=10.5��m��FeSO4��7H2O����m��Ni2+��=21����Ӧ�¶�Ϊ30 �棬n��Fe2+����n��Fe3+��=0.55 �������£��������ʱ���Ni2+ȥ���ʵ�Ӱ�죬�����ͼ6��
|
|
ͼ6 ����ʱ���Ni2+ȥ���ʵ�Ӱ��
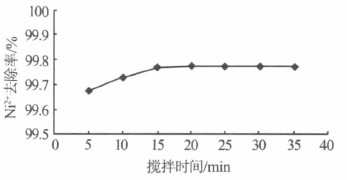
��ͼ6 ��֪����ˮ��Ni2+��ȥ�������Ž���ʱ������Ӷ����ӣ�������ʱ���l5 min ʱ��Ni2+��ȥ���ʻ������䣬�����������������ȶ��ĺ�ɫ�����壬��Ӧ�ѻ�����ȫ����������ӽ���ʱ�䣬Ni2+ȥ���ʵ��������ԡ��ۺϿ��ǣ�ѡ����ѽ���ʱ��Ϊl5 min��
3 ����
���������巨�Ը�Ũ�Ȼ�ѧ������ˮ������Ԥ������ͨ������ʵ��͵�����ʵ���о���pH��m��FeSO4��7H2O����m��Ni2+����n��Fe2+����n��Fe3+������Ӧ�¶Ⱥͽ���ʱ��Ի�ѧ������ˮ��Ni2+ȥ���ʵ�Ӱ�졣���������pH ����ҪӰ�����أ�����4 ������Ӱ����Խ�С����������ȷ���ι�ϵ����pH Ϊ10.50 ���ң�n��Fe2+����n��Fe3+��=0.55��m��FeSO4��7H2O����m��Ni2+��=21����Ӧ�¶�Ϊ30 �棬����ʱ��Ϊ15 min ����������£���ˮ�е�Ni2+��4 212.5 mg/L ����10 mg/L ���£�Ni2+ȥ���ʴﵽ99.75%���ϣ��÷���Ϊ���������춨�����õĻ�����
�÷��������豸��Ͷ�ʽ��٣��������ۺ����ã�������Ⱦ���ŵ㣬ֵ���ƹ㲢��һ���о�������