近年来,电镀工业迅速发展,电镀添加剂品种和数量日益增加,电镀添加剂生产废水已成为水环境的重点污染源之一。该废水具有有机物浓度高、成分复杂、可生化性差等特点,难以采用常规方法进行处理,且含有一些具有生物毒性或“三致"(致癌、致畸、致突变)性能[1-3]的有机物,一直是工业污水处理中的难点。
Fenton试剂是由H2O2和Fe2+复合而成的一种氧化能力很强的氧化剂。研究表明,H2O2和Fe2+之间产生羟基自由基.OH[4-6]。由于其具有极强的氧化能力,特别适用于生物难降解的或一般化学氧化技术难以奏效的有机废水的处理。同样,TiO2在紫外光的照射下也能产生.OH。本实验将两者结合,产生了很好的协同作用。
1.实验部分
1.1废水来源
实验水样来自广州市某电镀添加剂的企业生产废水(以下简称原水)。该水成分十分复杂,包含多种在生产过程中使用的添加剂产生的有机污染物。其初始COD高达7600mg/L,pH值为1.54。一般方法对其难以进行有效处理。
1.2实验仪器
多功能光化学反应仪(汞灯功率为300W),南京斯东柯电气设备有限公司;PHS-3C型pH计,上海精密科学仪器有限公司雷磁仪器厂;CJJ-6S数显磁力搅拌器,江苏麦普龙仪器制造有限公司;XJ-Ⅲ型消解仪,韶关市明天环保仪器有限公司;AL104型四位电子天平,梅特勒-托利多仪器(上海)有限公司;UV752型紫外可见分光光度计,上海佑科仪器仪表有限公司;飞鸽TGL-16C高速离心机,上海安亭科学仪器厂。
1.3实验试剂
30%H2O2,优级纯,成都市科龙化工试剂厂;FeSO4.7H2O,分析纯,天津市广成化学试剂有限公司;二氧化钛AEROXIDEP25,赢创德固赛;K2Cr2O7,分析纯,成都市科龙化工试剂厂。
1.4实验方法
取100mL原水加入250mL烧杯中,用H2SO4和NaOH溶液调节pH值后,边搅拌边依次加入一定量的FeSO4.7H2O颗粒和30%的H2O2。分别在一定时间取样,同时往样品中加入强碱溶液使其pH值超过10,一方面破坏Fenton试剂使反应停止,另一方面使Fe2+生成铁的氢氧化物沉淀从溶液中分离,避免Fe2+干扰COD的测定[7,8]。运用高速离心机离心样品,在转速为8000r/min的条件下离心,保证离心完全,取其上清液测定COD。
2.实验结果与讨论
2.1反应时间对COD降解的影响
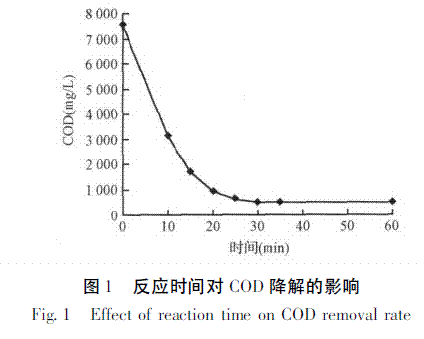
取100mL原水加入250mL烧杯中,调节pH为4,加入H2O210mL和FeSO4.7H2O1.2g。分别在10、15、20、25、30、35和60min取样测定其COD。由图1可知,反应时间为30min时,COD已降至最低,再增加反应时间,对COD的去除无影响。
2.2双氧水投加量对COD降解的影响
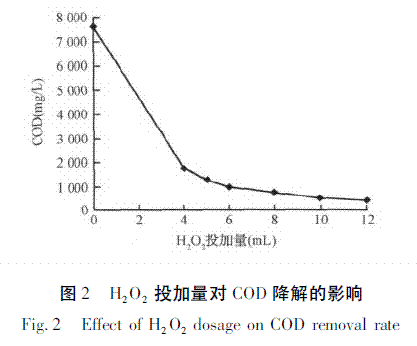
取100mL原水,调节pH为4,投入FeSO4.7H2O1.2g,分别加入4、5、6、8、10和12mLH2O2,取样时间设定为30min。由图2可知,随着H2O2投加量的不断增大,原水的COD下降的越多。这是由于反应持续进行,产生了大量的羟基自由基.OH,此外H2O2自身在紫外光照射下也能产生一定量的.OH。这些.OH很好地降解了废水中的有机物,进而使其COD不断降低。从图中可以看出,当H2O2投加量进一步加大时,COD的降低幅度大大减小。从经济角度考虑,H2O2的投加量存在一个最佳值,过量加入H2O2会加大处理成本,但对处理效果的进一步提高却并不明显。
2.3硫酸亚铁投加量对COD降解的影响
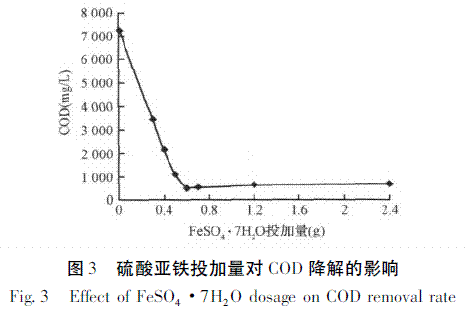
取100mL原水,调节pH为4,H2O2投加量为10mL,FeSO4.7H2O的投加量分别为0、0.3、0.5、0.6、0.7、1.2和2.4g,反应30min后取样,考察实验结果。由图3可知,如果Fe2+浓度较小,则不利于反应初始时羟基自由基或者别的活性氧化中间产物的产生;但也不是Fe2+越高越好,因为Fe2+浓度过大,一方面Fe2+和.OH结合生成了Fe3+,阻碍了氧化反应的进行。另一方面使H2O2消耗过快[9-11],而羟基自由基同原水中有机物的反应相对较慢,这样就使未消耗的游离羟基自由基积聚,这些羟基自由基彼此相互反应生成水2.OH+2.OH→2H2O+O[12-15]2。这两方面原因都降低了.OH的有效利用率,进而不利于COD去除的进行。所以说,Fe2+过低或过高都不利于氧化反应的进行。通过实验可得,该废水FeSO4.7H2O颗粒的最佳投加量为6g/L。此时,Fe2+和H2O2的摩尔比为1∶36。
2.4pH值对COD降解的影响
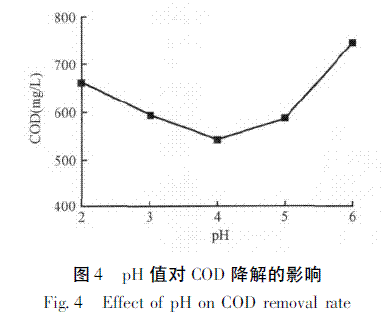
取100mL原水,H2O2和FeSO4.7H2O投加量分别为10mL和0.6g,调节废水的pH分别为2、3、4、5和6,反应30min后取样,考察实验结果。由图4可知,最佳pH=4。可能原因如下:如果pH值过低,Fe3+不能很好地还原成Fe2+,影响了Fenton反应的持续进行。如果pH值过高,使.OH的产率大大降低,且溶液中的Fe2+易以氢氧化物的形式沉淀而失去催化能力。
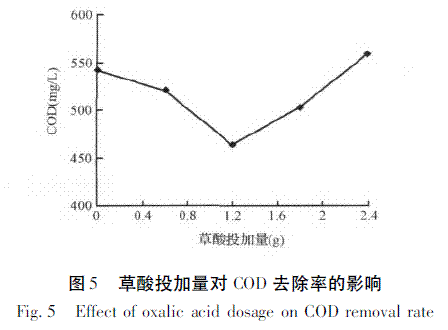
2.5草酸对Fenton反应的协同作用
取100mL原水,H2O2和FeSO4.7H2O投加量分别为10mL和0.6g,固定废水的pH为4,再分别投加草酸0.6、1.2、1.8和2.4g,反应30min后取样。由图5可知,一定量的草酸引入Fenton体系有利于反应的进行。草酸引入Fenton体系,草酸和铁离子混合后可形成稳定的草酸铁络合物Fe(C2O4)+、Fe[(C2O4)2]-和[Fe(C2O4)3]3-,以[Fe(C2O4)3]3-的光化学活性最强[16-18],它具有特殊的光谱特性,可以吸收高于200nm波长的光而产生.OH,反应式为:

2.6TiO2
对Fenton反应的协同作用设置好多功能光化学反应仪的相关参数,取300mL原水置于光反应器中,调节pH值为4,边搅拌边依次加入1.8g的FeSO4.7H2O颗粒、0.3gTiO2粉末和24mL30%的H2O2,立即打开300W汞灯照射。于60min时取样,同时往样品中加入强碱溶液使其pH值超过10。运用高速离心机离心样品,保证离心完全,取其上清液测定COD。
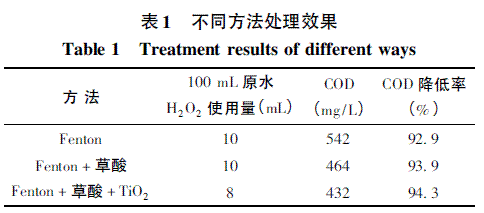
由表1可知,TiO2加入后,处理原水所消耗的H2O2减少,且处理效果也有一定程度的提升。这是因为TiO2与Fenton试剂之间存在着一种协同效应。TiO2对Fe3+的催化还原作用,提高了反应系统中Fe3+的浓度,促进了Fenton反应的进行,使系统中.OH的产率和浓度增大,氧化降解有机物的能力增强;另外,一方面电子接受体Fe3+的还原作用也有利于抑制TiO2光催化电子-空穴对的复合;另一方面,H2O2可与电子反应产生羟基自由基.OH,这也能抑制电子-空穴对的复合。这些都提高了TiO2本身的光催化量子效率。
3.结论
(1)有机物的降解主要依靠的是光-Fenton反应。投加高浓度的H2O2可以将大部分的有机物分解。当Fenton反应进行到一定阶段时,继续投加H2O2对于有机物的降解效果没有之前显著,而且成本提高太多。
(2)在Fenton反应之中投加一定量的草酸,一方面加速了Fe3+向Fe2+的转化,促进了Fenton反应的加速进行;另一方面反应过程中可以产生H2O2,从而可以减少废水处理过程中H2O2用量,降低废水处理成本。
(3)光TiO2催化反应与Fenton反应有很好的协同作用,但反应时间延长。通过实验,得出该废水的最佳操作条件:pH=4,H2O2投加量为80mL/L,FeSO4.7H2O投加量为6g/L,Fe2+与H2O2的摩尔比为1∶36,草酸投加量为12g/L,TiO2投加量为1.0g/L,反应时间为60min。经过处理,废水的COD从7600mg/L降至432mg/L,COD的降解率达到了94.3%。














