��Ϊ�ҹ�֧����Դ��ú̿�ڿ��ɹ����л��γɴ���ú�����Է�ˮ(acid mine drainage��AMD)������Ҫ�ص�ΪpH �ϵͣ�һ����4��5��6��5�����и�Ũ�ȵ������Σ������2 000��3 000 mg/L���Լ����ֿ����Ե��ж��ؽ������ӣ���Fe2+��Mn2+��Cu2+��Zn2+�ȣ��л���Ũ�Ƚϵͣ�һ��ú����COD��100 mg/L��1��2�ݡ���ЩAMD ��ֱ���ŷż��Ƕ�ˮ��Դ�ľ��˷ѣ�Ҳ������Ⱦ����������������Դ�ͳ���մ��ڸ߳ɱ���������Ⱦ�����⣬���òɿ�������ԭλ�����������Կ˷�����ȱ�㣬�һ����Ա��ֿ�������ˮ��Ȼƽ����һ���Ļ������ö���ΪAMD �����о�����Ҫ���ݡ�������Ӧǽ(permeable reactive barrier��PRB) ����ԭλ����AMD ��������ʱ�䳤����������ǿ��������ά������Ҳ���߾���Ч������ܹ�ע����Ч�Ļ��Բ�����PRB �ɹ�Ӧ�õĹؼ���
��ʯ(maifan stone��MFS) ��һ�ָƼ��ԡ������ҩʯ���ܹ��ͷ�Ca��Mg��Na��K��P �ȶ�������������ֳ�����Ԫ�أ��������õ������ܳ����ܣ������⽫����ΪPRB ���Բ��ϵ��о����б��������ڴ�ͳPRB ���ڶ���ֵ�AMD ��ҪӦ�ö��������ϵĸ��ϲ���ʵ�ֽϺõ��������ʩ��ά���Ѷȴ�Ҳ����֤���Բ��ϵij�Ч�ԡ���ˣ������������̶������������̶�SRB ���������MFS ��ΪPRB���Բ��ϣ�����Fe0 ��ʵ�����������Эͬȥ�ۡ���չ������̬�Ա�ʵ�飬ʵ��ģ���ϵͳ�Զ���֡��为��AMD �ij�����Ч����̽����������������ΪAMD �ͳɱ�����Ч�ȶ��ľ���ԭλ�����ṩ�·�����
1 ���ϼ�����
1��1 ʵ�����
ʵ������MFS ȡ���������£�����Ϊ30��60Ŀ��ʵ��ǰ������ˮ��ϴ2��3 ����ȥ������ҳ���105���ɺ���á�Fe0 ����Ϊ10��30 Ŀ��ʵ��ǰ��0��5 mol/L ��HCl ��Һ��ϴ2 h����ȥ�����������P���ۡ�ʵ���������ȡ�Ը����ɹ�����ˮ�����������أ�ʵ��ǰ����SRB ��������Һ��(35��1) �������������4 �ܺ�����������ȫ�����ƿ����Ũ�ҵij�������ζʱ��˵��SRB �ѳ�Ϊ�����е����ƾ��䡣
1��2 ʵ��װ�ù���
ʵ�鹲����3 ������Ϊ�л������ܡ��ھ�Ϊ55mm��PRB ��̬��������PRB-1��PRB-3 Ϊʵ������飬��350 mm��PRB-2 ��Ϊ450 mm��ÿ����Ӧ�������¶�װ��20 mm�ߡ�����Ϊ5��10 mm��ɰ�������㡣��PRB1��3 �ڸ�װ��߶�Ϊ200 mm�ľ���Ԥ������MFS��Ȼ�������Ӧ����ͨ��ģ��ˮ��������PRB-1��PRB-2 �ڽ���100 mL ��������������SRB ���֮࣬����PRB-2 ��װ��߶�100 mm����Ԥ������Fe0������ʵ�顣����Ӧ���ij�ˮ�ھ��߳����������ϱ���30 mm���Ա�֤���������Ļ�����ͬʱ�����Բ������������仯�����ʵ��װ�ü�ͼ1��
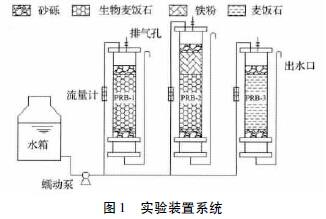
1��3 ʵ��ˮ��������
ʵ��ˮ������ijú���ˮ���ƣ����ݡ�ú̿��ҵ��Ⱦ���ŷű���(GB20426-2006)���ο�����ˮ�ۺ��ŷű���(GB8978-1996)���ÿ�ˮ��������Ⱦ����SO42-��Fe2+��Mn2+��NH3-N��pH ֵ��COD �ϵͣ���˸ÿ�ˮΪ�����������κ�������ú�����Է�ˮ��ʵ�鹲��3 �ν��У�I �ν�ˮ����Ⱦ���ɽϵͣ���ʹ����MFS ������Ӧ����������ǰ15 ��Ϊ�����Σ�15 d ǰ�����Ⱦ��ȥ���ʿ�ʼѸ��������������������ɡ�II �ν�COD/SO42-������2��0���ң�ͬʱ�����Ⱦ���ɣ�������̼Դ���������¸�ϵͳ����Ч����III �β�����ģ��ˮ����Ͷ��̼Դ��ͬʱ����ˮpH ����4 ���£�����ϵͳ�Ŀ��������������ʵ����6 ��4 �տ�ʼ����8 ��26 �ս�����ʵ���ڼ�����Ϊ25��35�棬������������ˮ������Ϊ0��1 m3/(m2��d)��ˮ����COD �������������ƣ�����ʵ������в�����Ͷ��SRB �����������Ԫ�ء�����ˮ��ָ�����1 ��ʾ��
��1 ����ˮ��

1��4 �����Ŀ������
COD: �ظ���ط�; SO42-: ���ᱵ�ֹ��ȷ�;Fe2+: �ڷƆ����ֹ��ȷ�; Mn2+: �ߵ���طֹ��ȷ�; NH3-N: �����Լ��ֹ��ȷ�; pH: �����缫����
2 ���������
2��1 pH �仯����
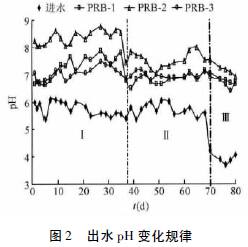
PRB-1 ��PRB-2 ��PRB-3 ������ʵ������г�ˮpH ƽ��ֵ�ֱ�Ϊ7��03��7��88 ��6��97����ͼ2 ��ʾ��PRB-2 ��pH ֵ����ͬ��ʱ����Ͼ���PRB-1��PRB-3��������ΪFe0 ���ˮ��H+��Ӧ�������������������е�pH ֵ���������Զ�SRB �����ƣ���ǿ���Ե�SRB �컯��лSO42-�Ĺ������ֲ��������ȣ���һ�������˳�ˮpH ֵ��PRB-1��PRB-3 ��pH ֵ������ʵ������м�����ȣ��ұ仯��С��������ΪMFS �Ļ�ѧ�������Al2O3����Al �ǵ��͵�����Ԫ�أ�����������·ֱ�����Al(OH)2+��H2AlO3-��ʽ���ڣ���˾������õ�pH˫�����������I ��֮����Ӧ����ˮ��pH ֵ�����½�������ԭ��Ϊ�����Ƚϸ�Ũ�ȵ�Mn2+�Ѷ�SRB ���������ԵĶ�������(��ͼ3(a) ��PRB-1��PRB-2 ��SO42-ȥ������II �εı仯����) ; ��νϸ�Ũ�ȵ�Fe2+�ٽ�������OH- ��ϵ�ˮ�����������Լ����������������Ũ�������ƵĹ����в��������ᣬҲʹpH ֵ�½���III �ν�ˮpHֵ���罵�ͣ�SRB ����Ҳ�ϵ�(��ͼ3(a) ��ʾ)�����Ǹ���Ӧ���ij�ˮpH ֵ��ά����7 ���ң����ֳ���pH ��ǿ�Ŀ��������������
2��2 SO42-��ȥ��Ч������
��ͼ3(a) ��֪��PRB-1 ��PRB-2 ��SO42-��ȥ���ʴӵ�7 �쿪ʼѸ����������15 d �ﵽ�ȶ���������Ӧ��������ɡ�����һ�����У�PRB-2 ��SO42-��ȥ���ʸ���PRB-1��������ΪFe0 ����ϵ�е��ܽ�����Ӧ�Ƚ���������ԭ��λ�ֿ��γ�����-��������������ˮ����ȥ��Mn2+��ΪSRB����Ӫ�������˵Ļ�����PRB-1 ��15 d ��I ��ĩ��SO42-��ƽ����ԭ����Ϊ120��15 mg/(L��d)���Ը���PRB-2��105��40 mg/(L��d) (����ȥ���ʾ�����60%) �����������ΪPRB-2 ��pH ֵ���ߣ�������SRB ���������ķ�Χ���¡�����II ��֮��PRB-2 ��SO42-��ƽ����ԭ����������456��60 mg/(L��d)����Ӧ��ƽ��ȥ����Ϊ58��76%��ȥ�����������ԭ��Ϊ������COD/SO42-������ΪSRB ��л��ṩ�˸��ӳ����̼Դ; �����һ����Χ��Խ��Ũ�ȵ�Fe2+�����ܴٽ�SRB �Ĵ�л������������H2S�������FeS �������ܼ��������Ķ������á�III ���ڲ���̼Դ�������£�PRB-2 ��SO42-��ƽ����ԭ���ʽ�����190��71 mg/(L��d)�����I�ζ����Ա����˽ϸߵĻ�ԭ���ʡ�PRB-1 ��I �κ��SO42-�Ļ�ԭ���ʼ�ȥ���ʶ��ձ����PRB-2������ʵ����PRB-3 ��SO42-��ƽ��ȥ���ʲ���10%���ɼ�MFS ��SO42-��ȥ�������ϵͣ����������ḻ�Ŀ��P���õ������ܳ������ܹ���֤�����ڲ������Ԫ�ص������¾��нϸߵĻ��ԣ����������Ϊ����̶�����������SRB ��������ΪPRB ���Բ��Ͻ���AMD ����ԭλ���ǿ��еġ�
2��3 COD ȥ��Ч������
��ͼ3(b) ��֪����I ��PRB-1��PRB-2 ��PRB-3��COD ƽ���������ʷֱ�Ϊ108��09��61��76��103��17mg/(L��d)������ǿ�����ò����ԡ�������Ϊ��һ����������Ҫ������Ϊ̼Դ����Fe0 �Ļ�ԭ����H2������������л����ΪSRB ��л�ĵ��ӹ��壬���Fe0 �Ĵ��ڿ��Լ���̼ԴͶ�����������ӱ���о�����һ�¡�����I �ε����������������е��л��������Ĵ�����PRB-1��PRB-2 ��II �ζ�COD �������ʷֱ�������614��26 mg/(L��d) ��410��42 mg/(L��d)������III �α��ֳ�2 �ֽ�Ȼ��ͬ�ı仯���ɣ�����ԭ�����Ϊû��Fe0 Эͬ��PRB-1 ��SRB ����Դ����ά�ִ�л���¡��ۺ�ͼ3(a) ��(b) ʵ�����ݿ�֪��PRB-2 ��II ��ʵ�����ĵġ�COD/��SO42-ԼΪ0��90��С��PRB-1 ��1��83����˴ӽ�Լ̼Դ�ɱ��ĽǶȳ���������PRB-2 ϵͳ�����������Խϵ͵�AMD ���л��������塣
2��4 Fe2+ȥ��Ч������
��ͼ3(c) ��ʾ������ʵ�������PRB-2 ��MFS��������ѧ�����������л�����³�ˮ������ⲻ��Fe2+�Ĵ��ڣ�ȥ����ʼ��ά����99��9% ���ϡ�PRB-1 ����15 d ����Ӧ�ں�Fe2+��ȥ������71��8%������94��20%��III ���ܵ��������Ӱ�콵��86��56%�����ͼ3 (a) �������֣��ڱ���ԭ��SO42-��Ħ������Զ���ڽ�ˮ��Fe2+��Ħ��������ǰ���£�PRB-1 ��û����PRB-2һ����ȫȥ��Fe2+��������д���һ��ʵ���о���PRB-3 ��I �ζ�Fe2+��ȥ����Ϊ87��17%����II��III ���Ա����˽ϸߵ�ȥ������(ȥ����Ϊ70��02%����) ��������ΪMFS ����ˮ�黷��ʱ�������������ӻ��������γɴ������Ի��ţ�-SiO�ݣ����Բ����ؽ�����ϸ������Ҳ��MFS �ܹ���Ϊ����̶������ԭ��֮һ��
2��5 Mn2+��ȥ��Ч������
��ͼ3(d) ��ʾ����I ��PRB-1 ��Mn2+��ƽ��ȥ����Ϊ42��76%�����ڶ��۵�ͨ��������ʵ��ó���ȥ���ʣ�����Զ����ͬһ��ϵ��Fe2+��ȥ���ʡ�Kevin ���о�������Mn2+������������Fe2+���ڵ�����º��ѽ��У���Mn2+�ļ�̬���ȶ��������γ��ȶ����ܵ����II ��PRB-1 ��Mn2+��ƽ��ȥ����ֻ��24��45%������PRB-3 ��33��61%��������ΪPRB-1 ��������MFS �ϵ�������ֳ������MFS �Ĵ������ܣ�����Ӱ���˶�Mn2+��������PRB-1 ��III �ζ�Mn2+��ȥ������II �κ��ڼ�����ȣ�COD/SO42-��pH ����Ӱ���С����ʱ��ϵ��Mn2+��Ҫ��SRB ϸ���ľ��������������������ñ�ȥ����PRB-2 �ڸ��ζ�Mn2+��ȥ���ʼ����������������Զ����ʵ������飬��ϵͳ�ڳ��˴��������MFS �������⣬Fe0 ��������������ԭ���γɵ�����-��������������ˮ�������ȥ��Mn2+�����ֳ����õ�����-������Эͬȥ��������
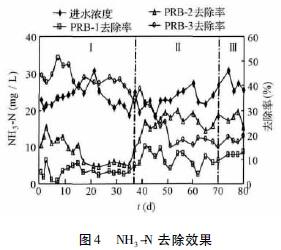
2��6 NH3-N ȥ��Ч������
��ͼ4 ��ʾ��PRB-1��PRB-2 ��I �ζ�NH3-N ��ȥ���ʵ���PRB-3��������ΪMFS �ڲ���������Ĵ��и���ɵ�����������ṹ��ʹ����Ϊ���ֵ����Զ���ϵĽ��������Ӽ�����ˮ��Һ����NH4+����������������������PRB-3 ��MFS ���и������Ч�ȱ�������������������ǿ���ɴ˿ɼ�������̶�����MFS �Ĵ������ܻ�����ϴ��Ӱ�졣I ��֮��PRB-1 ��ȥ����ҲѸ���½����������MFS ��Fe2+��Mn2+��������������NH4+�йء���ʵ�������PRB-2 ��NH4+��ȥ����һֱ����PRB-1����I ��֮��������PRB-3��������Ϊ��������������Fe0 ͨ����ѧ������������NO-3��ԭΪN2���������������Ի����·��ӵĸ�ǿ����ʵ���к��ڷ��֣�PRB-2 ���ڱ����н϶����Ҹ��ţ�����Ϊ��δ�����N2�����϶�����������ɫ���࣬Fe0 ��δ����������飬ϵͳ�Ծ������õ����ԡ�
3 ����
(1) MFS �������õ�pH �����������ܽ�pH ֵΪ3��7��6��1 ��AMD ���������Ի���ԣ�����MFSΪ���Բ��ϵ�PRB-3 ��Fe2+��Mn2+��NH3-N �����ȥ�����ʷֱ�Ϊ45��77��9��23 ��12��10 mg/(L��d) ��ͬʱ���õ������ܳ����ܼ���Ľṹ�ص�ʹ����Ϊ����̶���������й�����Ӧ��ǰ�������ǹ̶���֮����䴫�����ܾ���һ��Ӱ�졣�������SO42-��COD ȥ�������ϵͣ���˵�����MFS ��ΪPRB ���Բ����������AMD ���Դﵽ���õ�Ч������
(2) Fe0 ����������ǿ����MFS ��SRB ������������ͨ��������ѧ�����ֲ�ϵͳ������MFS ���������½��IJ��㡣��̼Դ����������(II ��) PRB-2��SO42-��Fe2+��Mn2+��NH3-N ���ȥ�����ʷֱ�Ϊ552��29��57��64��14��51 ��7��05 mg/(L��d) (��Ӧȥ���ʷֱ�Ϊ71��08%��99��9%��67��49% ��29��87%)��ȥ��Ч������PRB-1 ��PRB-3��ʵ���˶�����Ⱦ���ͬ��ȥ����
(3) Fe0 �Ļ�ԭ����H2�ܹ���ΪSRB ���ӹ��壬��֤��PRB-2 �ڲ���̼Դ�������(III ��) ��SO42-��Fe2+��Mn2+��NH3-N ���ȥ�����ʷֱ�Ϊ231��08��57��64��10��85 ��6��94 mg/(L��d)�����Fe0Эͬ����MFS ��PRB ϵͳ����ԭλ��AMD �ǿ��еġ�














