1 实验部分
1.1 仪器与试剂UV/Vis916型紫外 可见分光光度计(澳大利亚,GBC公司);723型分光光度计(上海第三分析仪器厂);501型超级恒温水浴(重庆试验设备厂)。铁(Ⅲ)标准溶液:用硫酸高铁铵配制1.0g/L的贮备液,使用时稀释成1μg/mL;孔雀绿溶液(MG):2.0×0.0001mol/L;H2O2溶液:10%;HCl溶液:1mol/L;琥珀酸二异辛酯碳酸钠溶液(AerosolOT):1.0×0.01mol/L;EDTA溶液:1.0×0.001mol/L。所用试剂均为分析纯,水为二次蒸馏水。
1.2 实验方法于两支25mL比色管中加入3.0mL2.0×10-4mol/L孔雀绿溶液(MG),1.0mL10%H2O2溶液,1.0mL1mol/LHCl溶液,1.6mL0.01mol/LAerosolOT溶液和适量铁标准溶液(条件实验加0.2μgFe3+),用水定容至刻度,摇匀,置80℃水浴中恒温15min,然后滴加0.001mol/LEDTA溶液0.5mL,冰水浴冷却20min,用1cm比色皿,波长615nm处以水为参比,测催化和非催化反应体系的吸光度A和A0,计算△A=A0-A。
2 结果与讨论
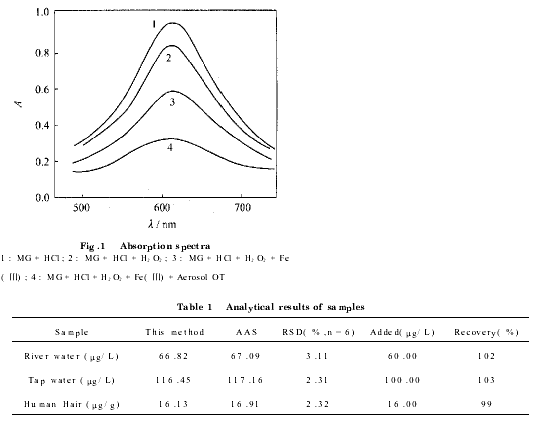
2.1 吸收光谱按实验方法配制不同组分溶液,绘制吸收曲线,见图1。曲线1、2表明H2O2能使孔雀绿溶液褪色,比较曲线2、3表明铁(Ⅲ)有催化作用,曲线3、4表明AerosolOT有增敏作用,所有曲线在615nm处均有最大吸收。所以,本法选择615nm作为测定波长。
2.2 溶液酸度的影响试验了稀盐酸、磷酸、乙酸 乙酸钠等多种介质,结果表明铁(Ⅲ)催化过氧化氢氧化孔雀绿这一指示反应,在1mol/LHCl溶液介质中最为强烈,其用量在0.8~1.2mL之间△A值最大重现性好。实验选用HCl溶液1mL控制体系的酸度。
2.3 表面活性剂的选择研究了溴化十六烷基吡啶、十二烷基磺酸钠、丙氨酸、甘氨酸、琥珀酸二异辛酯碳酸钠等对催化反应的影响,结果表明琥珀酸二异辛酯碳酸钠(AerosolOT)有增敏作用,增敏效果最佳。
2.4 试剂用量的影响按实验方法试验,结果表明当H2O2、MG和AerosolOT分别为0.8~1.2、2.6~3.4、1.4~1.8mL时,反应灵敏度高且重现性好。所以本法选择H2O2、MG和AerosolOT用量分别为1mL、3mL、1.6mL。
2.5 反应温度和褪色反应时间实验结果表明室温下本催化反应很慢,65℃以上催化反应速率明显加快,△A值也迅速增大,在80℃达到最大。温度进一步升高,非催化反应速率明显加快,△A值迅速变小。因此本法选择反应温度为80℃。80℃反应3~15min,△A值与反应时间t呈良好的线性关系。故本法选择加热时间为15min。2.6 终止反应与体系的稳定性由于室温下本催化反应很慢,可通过滴加EDTA溶液0.5mL,冰水浴冷却20min终止反应。10h内吸光度几乎不变,表明本催化体系具有很好稳定性。
2.7 动力学参数
2.7.1 反应级数与速率常数 反应时间为3~15min时,△A与反应时间t呈线性关系,表明该催化反应为假零级反应,线性回归方程为:△A=-3.9×0.01t+0.014,速率常数为3.9×0.01s-1。
2.7.2 表观活化能 根据70~80℃溶液吸光度随时间变化关系曲线,求出反应速率常数k,用-lnk对1/T作图得直线方程,求得表观活化能Ea=27.14kJ.mol-1。
2.8 工作曲线及检出限分别取不同量的铁标准溶液进行实验,铁含量在0~68μg/L范围内与△A值呈良好的线性关系,工作曲线回归方程为:△A=0.0425c(μg/L)+3.11×0.01,相关系数0.9996。用三倍的空白标准偏差除以回归方程的斜率(CL=3Sr/K)求得本法检出限为2.82×10-8g/L。
2.9 共存离子的影响当25mL溶液中含0.4μgFe(Ⅲ),测定相对误差≤±5%时,各共存离子的允许倍量为:K+、Na+、Ca2+、Li+、NO-3、Mg2+(1000);Ba2+、Br-、Zn2+、Pb2+、CO2-3、SO2-4、PO3-4(500);Cd2+、Co2+、W(Ⅵ)(300);Bi3+、Sn2+、Cr3+(100);Ag+、Ce3+、Hg2+(50);Cr3+、V(Ⅴ)(20);Mn2+、Ni2+、Cu2+(10)。常见离子都有较高的允许量,说明本法具有较高的选择性。
3 样品分析
3.1 水样取河水和自来水各25mL,加入10mL浓硫酸,加热蒸发至干,加水溶液定容至50mL。
3.2 人发样品称人发0.5000g,于5mLHNO3中浸泡过夜,加0.5mLHClO4,缓缓加热至冒白烟。冷却后用水冲洗并转移至容量瓶,用0.2mol/L的HCl定容。分别取经过处理后的溶液,稀释10倍后,按实验方法进行测定,分析结果见表1。