离心母液废水是采用悬浮聚合工艺生产聚氯乙烯(PVC)过程中产生的主要废水之一。该类废水具有水量大、浊度较高以及可生化性(BOD/COD)差的特点,属于低浓度难降解有机废水。废水的主要污染成分为用作分散剂的聚乙烯醇(PVA)。PVA 属于有机高分子类化合物,难以被生物降解。在水体中,PVA 通常以胶体状态存在,可形成大量泡沫并促进沉积的重金属迁移。因此,若直接大量排放含有PVA 的母液废水将带来严重的水体污染问题。自2006 年开始,我国PVC 产量跃居世界第一,仅2011 年我国因生产PVC而产生的母液废水总产量就约为5 200 万t,因此亟需一种高效、简便的母液废水处理方法。现阶段,常见的母液废水处理方法包括:混凝沉淀法、生物法、膜法等。但在应用上述方法处理母液废水时均一定程度地存在对可溶性COD 处理效率低、处理时间长及处理成本较高等问题。铁碳微电解法(又称内电解法、零价铁法等)因具有能耗低,处理效率高,能够提高废水可生化性等优点,近几年在印染、制药、农药、垃圾渗透液等难降解有机废水的处理中得到了广泛应用。微电解法的实质是原电池反应,其机理主要包括氧化还原、物理吸附、絮凝沉淀和微电场效应等多种物理化学作用。
本文采用铁碳微电解法对母液废水进行预处理研究,主要考察反应时间、铁粉投加量、Fe/C(质量比)、pH 以及曝气速率对废水中COD 及PVA 处理效果的影响,并通过正交实验确定母液废水的最佳处理条件。这在母液废水的处理中还未见报道。
1 材料和方法
1.1 废水的水质特征
本实验所用废水采自某大型氯碱化工企业的PVC 聚合工段。该企业采用典型的电石法悬浮聚合工艺进行PVC 生产。废水的部分重要水质指标如表1所示。
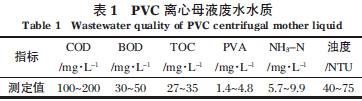
1.2 主要仪器及分析方法
仪器:COD 快速测定仪(美国哈希,DRB200);BOD 快速测定仪(美国哈希,Trak Ⅱ);便携式分光光度计(美国哈希,DB2800);总有机碳分析仪(日本岛津,TOC-L CPH);pH 计(PHS-3C)。
分析方法:COD 和BOD 采用快速测定仪测定。PVA 采用分光光度法测定。TOC 采用总有机碳分析仪测定。浊度、NH3-N 和总铁分别采用APHA 标准方法中的#2130B、#4500C 和#3500B测定。
1.3 实验方法
实验采用直径为50 mm,高为450 mm的有机玻璃管进行铁碳微电解法的静态单因素实验、正交实验及验证实验。实验开始前,将连接有胶管的曝气砂头置于有机玻璃管底部,胶管另一端依次连接流量计及空气泵。实验装置如图1所示。
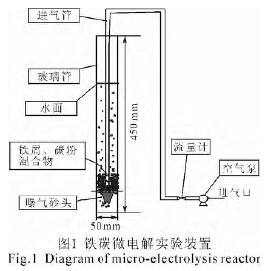
实验采用铁粉作为宏观阳极,大颗粒活性炭作为宏观阴极。实验前,活性炭用稀硫酸浸泡12h 后用去离子水反复清洗其表面污染物,然后进行饱和吸附以排除吸附作用对目标物质去除率测定结果的干扰。
1.3.1静态单因素实验
考察反应时间、铁粉投加量、Fe/C、pH、曝气速率对目标物质处理效果的影响。每组实验平行重复3次。具体实验过程为:将一定量的铁粉和活性炭的混合物及500 mL 已调节pH 后的母液废水由上方加入玻璃管内。将流量计调节至指定曝气速率后开始计时。当达到预定的反应时间后,调节废水的pH 至碱性进行絮凝沉淀。静置30 min 后取上清液过滤测定出水COD 和PVA 含量。所确定的各因素的初始条件为:铁粉投加量为30 g/L、pH 值=3、Fe/C 为1∶1、曝气速率为0.6 L/min。对每个影响因素进行优化时,首先固定其他因素,通过测定该因素取不同数值时相应废水的COD 和PVA 去除率,从而确定该因素的最佳值,再用此值取代初始条件中该因素的相应值,将修订后的条件作为下一个因素优化时的初始条件,直至完成所有因素的优化。各影响因素取值如下。反应时间:1、2、3、4、5、6h;铁粉投加量:2、4、10、21、30、40、50 g/L;Fe/C:3:1、2:1、3:2、1:1、2:3、1:2、1:3;pH:1、2、3、4、5、6、7;曝气速率:0.2、0.4、0.6、0.8、1 L/min。
1.3.2正交实验
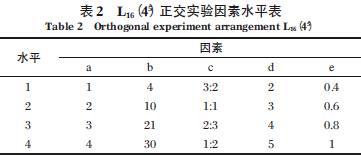
为获得最佳的处理效果,正交实验各影响因素的取值点在单因素实验所确定的平衡点附近选择。采用L16 (45)的正交实验表2 研究a:反应时间(h)、b:铁粉投加量(g/L)、c:Fe/C、d:pH、e:曝气速率(L/min)对COD去除效率的综合影响。每组实验平行进行3 次。正交实验因素及水平见表2。
1.3.3验证实验
将正交实验确定的最佳反应条件重复进行4 次,分别测定该处理条件下COD、PVA、TOC、NH3-N、浊度的去除率及总铁含量。
2 结果与讨论
2.1 静态单因素影响实验
2.1.1反应时间的影响
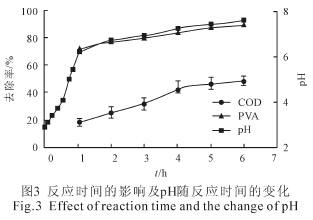
反应时间对母液废水COD 和PVA 去除率的影响如图3 所示。当反应时间达到4h 之前,二者去除率随反应时间的增加均呈现显著增加趋势,之后则趋于缓慢。该结果与其他的研究结果相似。
如图2 所示,PVA 的降解以[H]还原为主,・OH氧化为辅。在[H]或・OH 的作用下,PVA 首先脱掉一分子H2 或H2O 断链为含R・的小分子物质。R・经进一步的歧化或交互作用可生成酮或烯醇,并最终矿化。
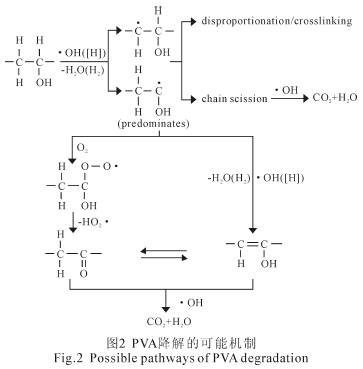
当反应时间较短时,体系内部产生的[H]、・OH 以及Fe2+的数量较少。此时,体系内氧化还原作用及后续的絮凝沉淀作用均不显著,因此对目标物质的去除率较低。随着反应时间的延长,COD 和PVA 的去除率趋于稳定。这主要是因为随着反应进行,体系逐渐增大的pH 加快了铁表面羟基化合物的形成,进而阻碍了铁单质与废水之间的电子迁移。此时,继续延长反应时间,目标物质的去除率将不再显著增加。由图3 可知,PVA 的去除率明显高于COD。这可能是由于相比于其他小分子有机物质而言,[H] 更易于与PVA 进行脱H2 反应。此外,相比于溶解态的有机物而言,铁离子的羟基络合物对胶体态PVA 的絮凝沉淀效果也更好。考虑到上述因素,之后实验的反应时间均选取4h。
2.1.2铁粉投加量的影响
铁粉投加量对COD 和PVA 的去除率的影响如图4 所示。COD 和PVA 的去除率随着铁粉投加量的增加均呈现先增加后稳定的趋势。当其投加量超过10 g/L 时,COD 和PVA 的去除率趋于稳定,分别为41%和78%。该结论与其他研究结果相似。
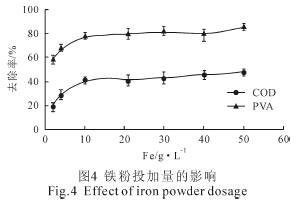
铁单质投加量是影响该方法去除率的重要因素之一。铁单质除可以与H+作用产生[H]外,还可以作为目标污染物质的氧化还原场所。当铁粉投加量过小时,体系内产生的[H]、铁离子数量以及所能提供的氧化还原场所均较少,对PVA 的脱氢、絮凝沉淀及氧化还原作用均较弱。因此,在此条件下PVA 的去除率较低。由反应体系COD/TOC 值较大(COD/TOC=5.1)可知,体系中还可能存在较多的含饱和烃链的物质。因此,在[H]较少的情况下,整个体系COD 的去除效率也较低。当铁粉投加量过大时,体系可在短时间内产生过量的[H]。由于[H]之间可形成H2,因此将减弱对体系内部的脱氢作用[6]。此外,瞬间积聚的过量Fe2+可以和・OH 反应,进而减弱对目标物质的氧化。研究表明,过量的铁单质可导致反应体系板结,进而降低处理效率[6]。综上所述,在后续实验中铁粉的用量选为10 g/L。
2.1.3 Fe/C 的影响
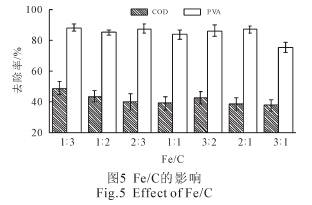
Fe/C 对反应的影响如图5 所示。随着活性炭含量的增加,COD 和PVA 的去除率整体上都呈现增加的趋势。
Fe/C 主要影响微电解反应中宏观原电池的形成及铁离子的溶出速率。当Fe/C 较大时,单位体积内铁粉和活性炭混合不均,形成的原电池数量较少,电化学作用较弱。因此,COD 和PVA 的去除率较低。研究表明,当采用未处理的活性炭的含量增加到一定程度时,活性炭对有机物的吸附成为主导作用。吸附作用除了对有机物的去除率小于微电解作用外,还能抑制微电解反应。因此,活性炭的含量不宜过高。不同于其他研究结果,本实验在Fe/C 较小时处理效果较好。这可能主要是由于本研究采用铁粉为阳极而导致的。相对于相同质量的铁屑而言,铁粉的比表面积更大,因此产生的宏观原电池更多。鉴于上述原因,后续实验中Fe/C 选为1∶2。
2.1.4 pH 的影响
pH 对反应的影响如图6 所示。当pH<2 时,COD和PVA 的去除率较高。随着pH 值的增大,COD 和PVA 去除率呈现逐渐减小的趋势。该结果与其他研究结论相似[13,25]。
如式(1)所示,H+直接参与铁碳微电解反应,因此其大小对目标污染物去除率的影响至关重要。
O2(g)+4H+(aq)+4e→2H2O(E=+1.23 V)(1)
O2(g)+2H+(aq)+2e→2H2O2(aq)(E=+0.68 V)(2)
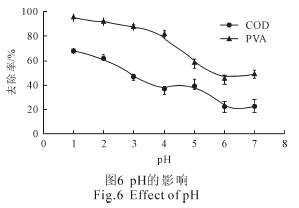
此外,pH 的大小影响PVA 的存在形态、阳极铁离子的溶出速率及[H]的数量。当pH 较低时,PVA 溶解度较低[11, 26]。此时,Fe2+的溶出速率较快并可产生大量的[H][20]。因此,体系内部的脱氢作用和絮凝沉淀作用较为显著。此外,较低的pH 可减弱铁离子的羟基络合物对铁表面的隔离作用,为有机物提供更多的氧化还原场所。但是,pH 也不是越低越好。当pH 过低时,该方法对目标物质的去除率趋于稳定。此时,继续降低pH值将消耗大量的酸,并导致阳极铁的过量溶解。不管是酸的消耗,阳极的消耗,还是由于阳极Fe 过量溶解而在随后过程中产生的过量Fe(OH)2 及Fe(OH)3 沉淀的处理,都将增加处理的成本,进而降低该方法的性价比。综合考虑处理效率及成本,后续实验选择在pH=2 的条件下进行。
2.1.5曝气速率的影响
曝气速率对COD 和PVA 去除率的影响如图7所示。COD 的去除率随着曝气速率的增加呈现先增加后降低的趋势。当曝气速率为0.8 L/min 时,其去除率为67%。PVA 去除率随着曝气速率的增加呈现先增加后稳定的趋势,当曝气速率达到0.6 L/min 左右时,其去除率为94%。
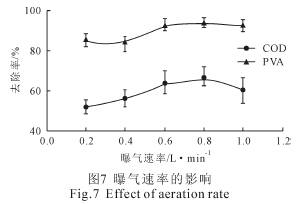
由式(1)、(2)知,曝气不仅可以提高体系的氧化性(E=1.23 V),还可产生少量的H2O2。由于Fe2+的存在,体系内部可以形成少量的Fenton 试剂,进而产生具有更强氧化性的・OH(E=2.80 V)。曝气还可加速Fe3+的形成。与Fe2+相比,Fe3+具有更好的絮凝沉淀效果[11]。然而,当曝气速率过大时,除空气中的O2 将减弱[H]对有机物的还原作用外,体系内HCO3-等・OH自由基清除剂的数量也将增加,进而减弱体系内部的氧化作用[2]。因此,当曝气速率超过0.8 L/min 时,COD去除率呈现了降低的趋势。综上所述,曝气速率应选择0.8 L/min。
2.2 最佳实验条件的确定
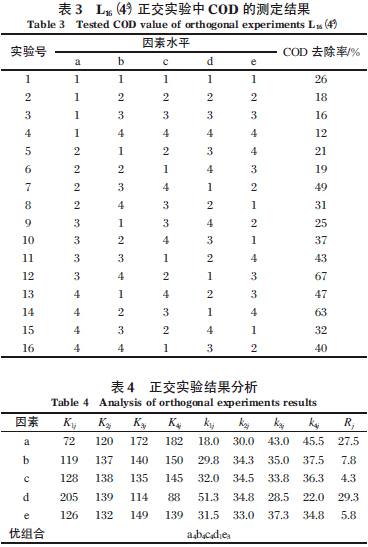
由L16(45)正交表所得的各实验条件下COD 的去除率列于表3 中。根据表3 可计算出Kij、kij 及Rj,具体结果列于表4 中。其中,Kij 为第j 列因素第i 水平所对应的COD 去除率之和(其中i=1,2,3,4;j=a,b,c,d,e); kij 为Kij 的平均值;Rj 为第j 列因素的极差。由表4可知,本实验所优化的5 个影响因素在所选择的取值范围内对母液废水COD 去除率影响的顺序为Rd=29.3>Ra=27.5>Rb=7.8>Re=5.8>Rc=4.3,即pH 对COD去除率的影响最大,其次是反应时间。铁粉投加量、曝气速率以及Fe/C 对COD 去除率的影响相对较小。在本实验所选的优化参数中,最佳因素组合为a4b4c4d1e3,即反应时间为4h,铁粉投加量为30 g/L,Fe/C 为1∶2,pH 值为2,曝气速率为0.8 L/min。。
2.3 最佳条件下的处理结果
在上述最佳处理条件下,处理后母液废水中COD、PVA 和TOC 的平均去除率分别为(67±2)%、(98±1)%和(55±3)%,BOD/COD 值从0.3 提高到0.5,可生化性得到了显著提高。此外,由处理前后废水的COD/TOC值由5.1 降到3.8 可以看出,该处理条件对含有饱和烃链类物质或其他H 元素含量较高的类似物质有很好的去除效果,这也可能是体系可生化性提高的原因之一[28]。此外,母液废水中的NH3-N 和浊度也同时得到了一定程度的去除,其去除率为45%和100%。虽然该方法中铁单质的溶解会导致出水中含有铁离子,但测定结果表明,经过沉淀后出水中总铁含量很低。与现阶段应用较为广泛的膜法以及传统生物法相比,铁碳微电解法除具有处理时间短、处理成本低的优点外,还克服了在采用上述2 种方法处理母液废水时存在的膜堵塞以及微生物不易培养的缺点。此外,铁碳微电解法还可以与Fenton 法及O3 氧化法联合使用,进一步提高对目标污染物的处理效率,降低处理成本。














